Figura 24
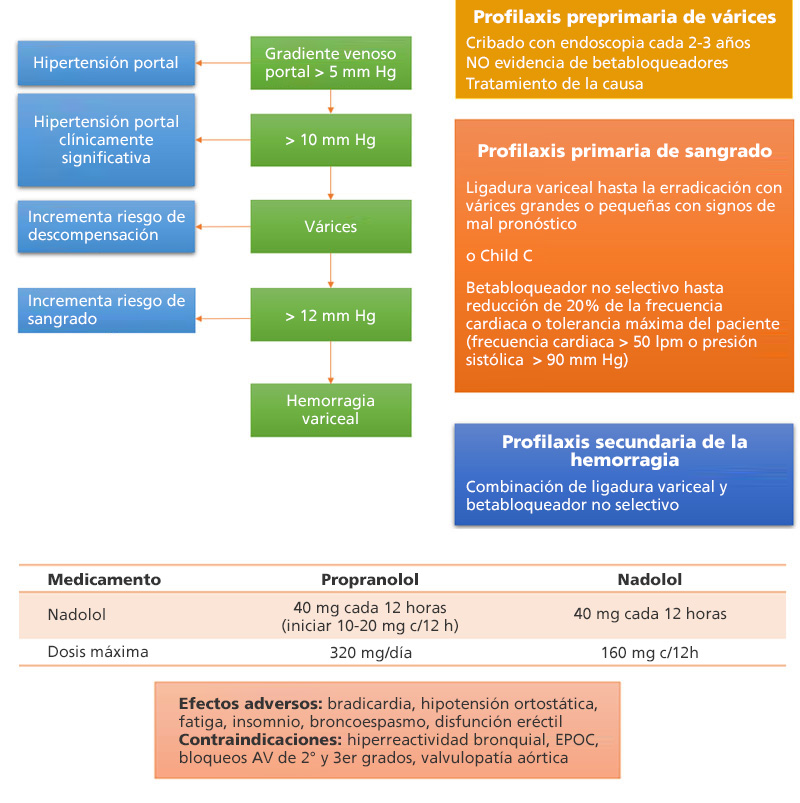
Tratamiento de cirrosis hepática. (Modificado de Tsochatzis EA, Bosch J, Burrough AK. Liver cirrhosis. The Lancet. 2014 May 17;383:1749-1761.)
Coordinador: Dr. Juan Miguel Abdo Francis
Cirrosis
Dr. José Luis Pérez Hernández
Durante decenios el término cirrosis se ha utilizado para definir la culminación de enfermedades hepáticas crónicas de diversas etiologías. La "cirrosis" (en griego "κίρρος" – coloración amarillenta o marrón), inicialmente se usó para caracterizar la morfología nodular y firme del hígado en los pacientes con enfermedad hepática. La definición de Sheila Sherlock de cirrosis hepática se basó en la morfología: un proceso difuso de fibrosis y formación de nódulos. La fibrosis extensa y la arquitectura lobular y vascular alterada provocan hipertensión portal progresiva y disfunción hepática.1
La cirrosis hepática representa la séptima causa de muerte en mujeres y la cuarta causa de muerte en hombres según las estadísticas de 2015.2 La etiología puede ser diversa; sin embargo, a nivel mundial la etiología viral suele ser la más común siendo la decimocuarta causa de muerte, mientras que en México la causa más común de hepatopatía crónica es el consumo crónico de alcohol, compitiendo de manera revolucionada con la esteatohepatitis no alcohólica, asociada a la epidemia de obesidad y síndrome metabólico.2
Otras causas y tratamientos de cirrosis se enmarcan en el Cuadro 18.
| Cuadro 18. Causas y tratamientos de cirrosis | |||||
| Etiología | Tratamiento | ||||
| Hepatitis viral | Hepatitis B | Continuar supresión de la replicación viral con análogos de nucleotidasa | |||
| Hepatitis C | Antivirales de acción directa hasta erradicar | ||||
| Hepatopatía por alcohol | Abstinencia | ||||
| Enfermedad por hígado graso no alcohólico | Tratamiento síndrome metabólico | ||||
| Hepatitis autoinmune | Esteroide y terapia inmunosupresora | ||||
| Metabólicas | Hemocromatosis | Flebotomías, quelantes de hierro | |||
| Enfermedad de Wilson | Quelantes de cobre | ||||
| Deficiencia α1-antitripsina | Trasplante | ||||
| Glucogenosis tipo IV | Trasplante | ||||
| Drogas hepatotóxicas | Identificación del factor desencadenante | ||||
| Síndromes colestásicos | Colangitis biliar primaria | Ácido ursodesoxicólico | |||
| Colangitis esclerosante primaria | Trasplante | ||||
| Síndromes de sobreposición | Ácido ursodesoxicólico e inmunosupresores | ||||
| Cirrosis biliar secundaria | Reconstrucción o derivación vía biliar | ||||
| Obstrucción de flujo venoso | Síndrome de Bud-Chiari | Recanalización del flujo venoso, trasplante | |||
| Cirrosis cardiaca | Tratamiento de la cardiopatía | ||||
| Criptogénica | Tratamiento de las complicaciones | ||||
| Modificado de Ivanova I. Liver cirrhosis: New concepts. Scripta Scientifica Medica. (2016). 48. 10.14748/ssm.v48i2.1481. | |||||
Los mecanismos fisiopatológicos que promueven el hígado cirrótico son la inflamación y necrosis persistente con acumulación de la matriz extracelular desorganizada (fibrosis) con capilarización de sinusoides, reorganización vascular, trombosis, obliteración, recanalización de venas y derivaciones arteriovenosas, formación de nuevos vasos y colaterales, así como regeneración. Todo ello perpetuado por desequilibrio de fibrogénesis y mediadores inflamatorios celulares.3,4 Promoviendo que las células estrelladas y los fibroblastos mantengan regeneración parenquimatosa en los hepatocitos lo que deriva en insuficiencia del funcionamiento hepático e hipertensión portal.3,4
El hígado complementa múltiples funciones, es el principal órgano que se encarga de metabolizar hidratos de carbono, lípidos y proteínas; se encarga del catabolismo de hormonas como insulina, glucagón, somatomedinas, producción de hormonas sexuales, metabolizante de glucocorticoides, hormona tiroidea, prolactina, hormona de crecimiento; catabolismo y almacenamiento de vitaminas como D, K, A, ácido fólico y vitamina B; metabolismo de bilirrubina y ácidos biliares; metabolismo y eliminación de fármacos y tóxicos; función de almacenamiento.5
Todas estas funciones se ven mermadas por la presencia de depósito extracelular y la reducción de la masa hepática.
El pronóstico de la hepatopatía puede agruparse según la clasificación de Child-Pugh-Turcotte o por el modelo de MELD para determinar el deterioro de la hepatopatía así como el riesgo de fallecer (Cuadro 19).5
| Cuadro 19. Clasificación Child-Pugh-Turcotte | |||
| VARIABLE | 1 PUNTO | 2 PUNTOS | 3 PUNTOS |
| Bilirrubinas (mg/dL) | < 2 | 2-3 | > 2 |
| Ascitis | Ausente | Leve o moderada | Tensión o refractaria |
| TP (INR) | < 1.7 | 1.7-2.3 | > 2 .3 |
| Encefalopatía | Ausente | Leve (I-II) | Grave (III-IV) |
| Albúmina (g/L) | > 3.5 | 3.5-2.8 | < 2.8 |
El depósito de matriz extracelular promueve la distorsión de la arquitectura lobular y vascular, lo que genera mayor resistencia intrahepática que conduce a hipertensión portal, misma que se define como presión portal mayor a 5 mm Hg.6 Las complicaciones secundarias a la hipertensión portal generan manifestaciones clínicas al alcanzar el umbral de 10 mm Hg y se denomina "hipertensión portal clínicamente significativa”.1,7
La hipertensión portal conlleva a vasodilatación de la arteria esplácnica, con secuestro de volumen circundante efectivo, activando mecanismos compensatorios, incremento del gasto cardiaco y el sistema renina-angiotensina-aldosterona lo que promueve retención de sodio y agua perpetuando la formación de ascitis, deterioro del funcionamiento renal y falla cardiaca.7
Etapa asintomática, son pacientes que se encuentran con estadio de Child-Pugh A con requerimiento de seguimiento y vigilancia o tratamiento de la causa desencadenante. Con prevención de hepatocarcinoma.1,7
Sintomática, se define por la evidencia clínica de las principales complicaciones de la cirrosis dados por estadio B o C de Child-Pugh: ascitis; encefalopatía hepática; hemorragia gastrointestinal e ictericia.1,7
La progresión de esta fase descompensada puede acelerarse por otras complicaciones como: peritonitis bacteriana espontánea, la ascitis refractaria, síndrome hepatorrenal, síndrome hepatopulmonar, infecciones sistémicas.
Es necesario tener en cuenta el término de insuficiencia hepática aguda sobre crónica que se caracteriza por deterioro agudo del funcionamiento hepático en pacientes con hepatopatía crónica, precipitado por un factor con daño multiorgánico y un alto riesgo de muerte a corto plazo.6
No olvidar que el riesgo de carcinoma hepatocelular (CHC) puede ocurrir en todas las etapas de la enfermedad, por lo que es necesario mantener en vigilancia.6
La formación de várices esofágicas es la primera consecuencia clínicamente relevante de la hipertensión portal. Actualmente se recomienda que todos los pacientes con cirrosis deben ser examinados para detección de várices. El crecimiento variceal es del 7% por año y el 12% de sangrado por año.6-8
El desarrollo de várices se relaciona al grado de Child-Pugh estimando el 40% de los pacientes en estadio A, el estadio B el 60% y C el 85%. Las várices gástricas pueden encontrarse hasta en el 33% de los pacientes. Con alto riesgo de sangrado várices mayores de 5 mm, así como presencia de puntos rojos.6-8
Por eso el tratamiento se esquematiza en el flujograma (Figura 24).5,8
Figura 24

Tratamiento de cirrosis hepática. (Modificado de Tsochatzis EA, Bosch J, Burrough AK. Liver cirrhosis. The Lancet. 2014 May 17;383:1749-1761.)
La cirrosis, la hipertensión portal, así como la persistencia de vasodilatación esplácnica por aumento de óxido nítrico, es el principal mecanismo fisiopatológico de ascitis. Con la progresión de la cirrosis, la activación de sistemas compensatorios promueve la retención de sodio, agua y, finalmente, el líquido retenido se acumula en la cavidad peritoneal como resultado del aumento de la presión portal.9
La supervivencia a un año de los pacientes que desarrollan ascitis disminuye al 50%, en comparación con la supervivencia de 90% a un año de cirróticos compensados.1,9
Tratamiento con la implementación de diuréticos, vigilancia del funcionamiento renal e hidroelectrolítico y restricción de sodio dietético.9
El desarrollo de encefalopatía es un signo clave y de mal pronóstico en los pacientes con cirrosis ya que la tasa de mortalidad asociada a 1 año es de hasta el 64%.10
Constituye un espectro de alteraciones neuropsiquiátricas con mecanismo fisiopatológico aún en estudio. Las características de reversibilidad y la ausencia de alteraciones anatómicas sugieren un trastorno metabólico que se fundamenta en neurotoxicidad mediado por el glutamato que constituye el principal neurotransmisor excitatorio del cerebro, es un importante metabolito y está involucrado en la fijación de amonio en el cerebro, traslocado a la circulación desde la luz intestinal; sin embargo, el uso de diuréticos e infecciones también puede desencadenarla.10,11 La lactulosa es el fármaco de primera elección para la prevención de la encefalopatía. La L-ornitina-L-aspartato es equivalente a la rifaximina, un antibiótico no absorbible, es eficaz cuando se agrega a la lactulosa si la encefalopatía recurre.11