Figura 21
Índice de actividad de la colitis ulcerosa crónica idiopática de Truelove-Witts. Fuente: Hanauer SB. N Engl J Med. 1996;334(13):841-8.
Coordinador: Dr. Juan Miguel Abdo Francis
Colitis ulcerosa crónica idiopática
Dr. Luis Charúa Guindic, Dra. Teresita Navarrete Cruces
La colitis ulcerosa crónica idiopática (CUCI) es una enfermedad de etiología aún desconocida, que involucra una desregulación del sistema inmune relacionado con factores genéticos y ambientales. El diagnóstico lo establecen la historia clínica, el examen físico, los hallazgos endoscópicos e histopatológicos.
Junto a la enfermedad de Crohn y la colitis indeterminada, la CUCI se engloba dentro de la denominada enfermedad inflamatoria intestinal, dada la similitud en ciertos aspectos patogénicos, evolutivos y de respuesta al tratamiento.
Su incidencia es mayor en los países de altos ingresos, es más común en Inglaterra, Noruega y Suecia al compararse con los países del sur de Europa; la incidencia más alta se encuentra en Islandia con 24.5/100 000 habitantes. En Norteamérica la incidencia es del 2.2 al 14.3 casos por 100 000 habitantes/año y la prevalencia de 37 a 246 casos por 100 000 habitantes/año. En México se calcula una incidencia del 0.2 al 4.89% y no se tiene conocimiento preciso de la prevalencia en la población adulta. En un estudio realizado en el Instituto Nacional de Ciencias Médicas y Nutrición se encontraron, en un periodo de 20 años, 848 nuevos casos, con un aumento en la atención de pacientes con esta enfermedad en el segundo decenio del estudio. En el Hospital General de México, en un periodo de 14 años, se diagnosticaron 200 casos. La enfermedad afecta en igual número a hombres y mujeres, con dos picos de incidencia máxima: el primero entre los 15 y 30 años y el segundo, de los 55 a los 80 años.
Dentro de los factores de riesgo identificados para desarrollar este padecimiento está el antecedente familiar de enfermedad inflamatoria intestinal, el consumo de grasas monoinsaturadas y poliinsaturadas y de vitamina B6. El tabaquismo parece ejercer un efecto protector en el desarrollo de la colitis ulcerosa y está asociado a un curso más leve; en Francia un estudio mostró que los fumadores tienen menor actividad de la enfermedad, menor número de hospitalizaciones y menor uso de corticoesteroides e inmunomoduladores. Esta observación no se ha demostrado con la utilización de parches de nicotina, probablemente por una menor dosis. Un paciente con apendicectomía (por apendicitis verdadera) tiene menos riesgo de padecer la enfermedad (69% de reducción).
La enfermedad se caracteriza por una inflamación crónica de la mucosa colorrectal, con periodos de exacerbación y remisión, que siempre abarca el recto y de ahí se extiende proximalmente, afectando porciones variables de la mucosa colónica. En promedio del 50 a 80% de los pacientes presentarán recaídas cada 4 a 12 semanas y 15 a 30% se encontrarán crónicamente activos.
El síntoma más característico de la CUCI es la diarrea con sangre. Pueden añadirse otros síntomas, como fiebre (en especial en las formas extensas), dolor abdominal, síndrome rectal (tenesmo, urgencia al evacuar y esputo rectal de sangre y moco) y pérdida de peso. Además, pueden aparecer múltiples manifestaciones extraintestinales de la enfermedad, siendo las más frecuentes las articulares (artralgias, artritis) y las cutáneas (eritema nodoso, pioderma gangrenoso).
De acuerdo con su extensión, evaluada a través de un estudio endoscópico, se clasifica según los criterios de Montreal en proctitis cuando únicamente hay afección del recto, colitis izquierda cuando se extiende hasta el ángulo esplénico, y extensa cuando la enfermedad afecta el colon más allá del ángulo esplénico. La colitis extensa se presenta en 20% de los pacientes y la colitis izquierda comprende del 50 al 60% de los casos. La extensión de la enfermedad determina la modalidad del tratamiento (tópico y/o vía oral) y la frecuencia e inicio de la vigilancia para cáncer.
Los cambios endoscópicos característicos comienzan cerca de la línea anorrectal y se extienden proximalmente en forma continua, confluente y concéntrica. El límite entre la mucosa inflamada y normal suele estar bien definido y puede ocurrir abruptamente en milímetros, especialmente en la enfermedad distal. Los aspectos endoscópicos de inflamación leve son eritema, congestión vascular de la mucosa y pérdida de la red vascular. La colitis moderadamente activa se caracteriza por ser granular y áspera, con erosiones y fragilidad mucosa al simple contacto. La colitis severa se caracteriza por hemorragia espontánea y ulceración. En la enfermedad de larga evolución, la mucosa se atrofia y se pierden las haustras con estrechamiento de la luz y seudopólipos.
Durante los brotes agudos de actividad, la mucosa presenta un importante infiltrado inflamatorio compuesto por linfocitos y células plasmáticas, junto a neutrófilos que aparecen predominantemente en las criptas, formando abscesos crípticos muy característicos, pero no patognomónicos. Asimismo, las criptas presentan distorsión estructural, disminución de sus ramificaciones y de células caliciformes.
Durante las fases de remisión, disminuye o desaparece el infiltrado inflamatorio y los abscesos crípticos, y se recupera el número de células caliciformes; sin embargo, las criptas persisten distorsionadas, acortadas y con una menor ramificación.
Sin importar la extensión de la enfermedad el riesgo de desarrollar cáncer colorrectal es del 2% a los 10 años, del 8% a los 20 años y del 18% a los 30 años (0.4% por año); los pacientes que tienen mayor riesgo de desarrollar cáncer son aquellos con una afección extensa del colon, 8 o más años de evolución de la enfermedad, antecedente familiar de cáncer colorrectal, colangitis esclerosante primaria e inicio de la colitis a edad temprana. Se denomina colitis ulcerosa de larga evolución, en el caso de la colitis extensa, cuando es mayor de 8 años y de 10 cuando sólo es del lado izquierdo. Se recomienda vigilancia con colonoscopia y toma de biopsias a los 8 años de haber iniciado con la enfermedad para los pacientes con pancolitis y después de los 10 años para los portadores de colitis izquierda; la frecuencia del estudio endoscópico dependerá de los hallazgos de las biopsias.
Si las biopsias son negativas a displasia, se pueden realizar de 1 a 2 años; después de dos colonoscopias negativas, pueden espaciarse hasta 3 años hasta que se cumplan 20 años con el padecimiento; posteriormente se continuará con el seguimiento cada 1 a 2 años. En caso de encontrar displasia de alto grado en mucosa plana se sugiere tratamiento quirúrgico. Pacientes con estenosis en algún segmento del colon, es indispensable tomar múltiples biopsias para descartar carcinoma; el 24% de ellas presentan malignidad. Cuando se encuentra displasia de bajo grado se puede recomendar la cirugía como profilaxis para evitar la progresión de la displasia; sin embargo, si el paciente no acepta, un seguimiento con colonoscopia cada 3 a 6 meses es una conducta aceptable.
En todos los casos de pacientes con displasia, de cualquier grado, la biopsia debe ser evaluada por un segundo patólogo experto en tejido gastrointestinal. En los pacientes con colangitis esclerosante primaria se sugiere iniciar al momento del diagnóstico de este padecimiento con seguimientos anuales. Cuando la enfermedad es sólo proctosigmoiditis (sin afección proximal a los 35 cm), la vigilancia se realiza de acuerdo a los criterios establecidos para tamizaje de cáncer colorrectal en la población en general. Una vez que el paciente se encuentra en remisión es innecesario realizar colonoscopias frecuentes; se deberán empezar según el esquema de seguimiento. En los casos con recaída, pacientes dependientes de esteroides o refractarios a los mismos, o cuando se considera realizar cirugía, es conveniente realizar una colonoscopia.
Es preferible que en el paciente con actividad moderada o severa, se disminuya la gravedad del padecimiento antes de realizar la colonoscopia. En caso de que una estenosis no permita el paso del endoscopio, el colon por enema de bario y la colo-TC (colonografía por tomografía computada) ayudarán a precisar las características de la lesión. La confirmación histológica es fundamental para el diagnóstico, hasta en el 10% de los pacientes durante los primeros 5 años de su enfermedad puede cambiar el diagnóstico histopatológico por enfermedad de Crohn o de colitis indeterminada.
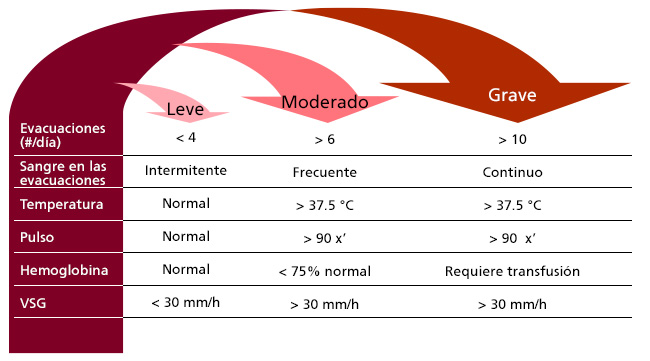
La gravedad del padecimiento se evalúa a través de diferentes escalas en: remisión, leve, moderado y grave; la definición de remisión más utilizada es la presencia de ≤ 3 evacuaciones al día sin sangre y sin urgencia. Múltiples escalas se han creado para determinar la actividad de la enfermedad, información que es necesaria para iniciar el tratamiento de los pacientes y determinar si una vez iniciado está siendo efectivo. Los parámetros propuestos por Truelove y Witts son los utilizados en la mayoría de los centros hospitalarios para realizar una evaluación clínica diaria (Figura 21). Sin embargo, la escala de Mayo es una opción adecuada y más completa, por el hecho de incorporar en los mismos parámetros la friabilidad de la mucosa evaluada por colonoscopia o rectosigmoidoscopia (Figura 22).
Figura 21

Índice de actividad de la colitis ulcerosa crónica idiopática de Truelove-Witts. Fuente: Hanauer SB. N Engl J Med. 1996;334(13):841-8.
Figura 22
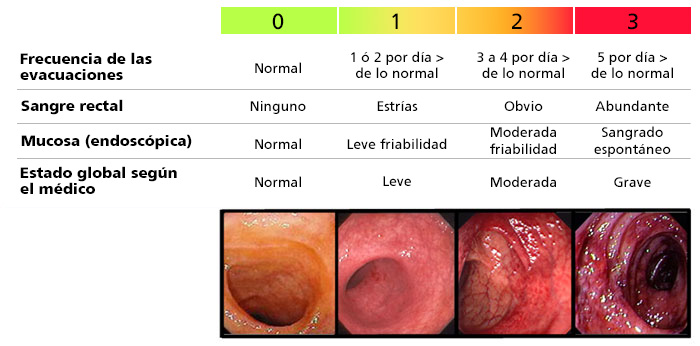
Escala de Mayo.
Los criterios modificados de Baron se utilizan con bastante frecuencia para indicar la actividad de la enfermedad durante una sigmoidoscopía: Grado 1 (leve), sin hemorragia espontánea o al contacto ligero y no hay un patrón vascular visible; Grado 2 (moderado), hemorragia al contacto ligero, no hay hemorragia espontánea; Grado 3 (grave), hemorragia espontánea y al contacto ligero. Es importante asentar en las notas clínicas la gravedad del padecimiento y el medicamento al cual está respondiendo (mesalazina, esteroide, inmunomodulador o biológico).
La sintomatología del paciente casi siempre tiene relación con la extensión de la enfermedad y la gravedad del padecimiento; la hematoquecia, urgencia y tenesmo son datos que se presentan con mayor frecuencia en pacientes con proctitis. Las evacuaciones nocturnas y el dolor abdominal son datos clínicos de importancia, al igual que la fiebre, la anorexia y la astenia en casos graves o de pancolitis. El 90% de los pacientes presentan hematoquecia como signo inicial; la persistencia de evacuaciones disminuidas en consistencia por más de 6 semanas casi descarta origen infeccioso. El 15% de los pacientes inician con un padecimiento grave y en 10% se puede identificar una manifestación extraintestinal (artropatía axial o periférica, epiescleritis y eritema nodoso) durante el cuadro inicial.
Los estudios de laboratorio más utilizados para conocer la actividad de la enfermedad son la proteína C reactiva y la velocidad de sedimentación globular; sin embargo, la calprotectina, lactoferrina fecal, la elastasa y el S100A12, tienen un papel de mayor importancia en la evaluación de la gravedad de la enfermedad. Existe una producción muy alta de calprotectina y lactoferrina por los leucocitos. La calprotectina fecal es un componente antimicrobiano citoplásmico en los granulocitos, monocitos y macrófagos, sus niveles tienden a relacionarse directamente con la actividad de la enfermedad y la inflamación de la mucosa.
Por otra parte, la sensibilidad al utilizar la serología para p-ANCA y diferenciar colitis ulcerosa de enfermedad de Crohn es insuficiente; existen reportes de una sensibilidad del 60% y especificidad del 94% para CUCI. En Estados Unidos se cuenta con un panel de pruebas inmunológicas aplicadas a la enfermedad inflamatoria intestinal, Serología 7 para EII (IBD Serology 7, Prometheus Laboratorios Inc., San Diego, CA), el cual incluye IgA, ASCA, IgG ASCA, IgA, anti-OmpC, anti-CBir 1 y p-ANCA específico de EII; el laboratorio reporta una sensibilidad del 93% y especificidad del 95% de acuerdo con el patrón de valores de los anticuerpos encontrados.
En todos los pacientes, durante el cuadro inicial, se deben realizar coprológicos, coproparasitoscópicos y cultivos así como pruebas específicas para Campylobacter, Clostridium difficile y Escherichia coli O157:H7, Entamoeba y otros parásitos.
En los pacientes con actividad importante la colonoscopia está contraindicada por el riesgo de perforación; una rectosigmoidoscopia flexible es suficiente para valorar la gravedad; los hallazgos de la actividad grave por endoscopia incluyen despulimiento extenso de la mucosa y úlceras profundas con desgarro de la mucosa en los bordes de las úlceras. La colonoscopia virtual en pacientes con colitis ulcerosa en este momento no sustituye a la colonoscopia convencional. Las placas simples de abdomen ayudan a descartar megacolon o perforación.
Dentro de los indicadores importantes para evaluar la respuesta al tratamiento figuran: la disminución de la actividad en más del 30% según el índice utilizado, disminución de la hemorragia rectal y mejoría del subíndice endoscópico. La recaída (aumento de puntaje de la escala utilizada), es el incremento en la rectorragia, el aumento en el número de las evacuaciones y la friabilidad de la mucosa. La recaída temprana es cuando se presenta en un periodo menor a los tres meses de haber alcanzado una remisión. Una recaída infrecuente se presenta una vez al año, frecuente dos o más veces al año y es continua cuando no existen periodos de remisión.
La colitis refractaria a esteroide se presenta cuando después de 4 semanas con tratamiento de prednisolona (o equivalente) de 0.75 mg/kg/día el paciente continúa con actividad de la enfermedad. La colitis dependiente de esteroides es aquella que se activa dentro de los tres primeros meses de haber suspendido el esteroide, o cuando no se puede disminuir la prednisolona a menos de 10 mg/día dentro de los tres meses de haber iniciado el tratamiento.
En los casos que presentan reactivación o son refractarios al tratamiento es necesario realizar cultivos de materia fecal buscando infección por Clostridium difficile; una rectosigmoidoscopia flexible ayudará a descartar una colitis pseudomembranosa y en pacientes inmunocomprometidos (inmunomoduladores), descartar infección por Citomegalovirus.
El tratamiento vía rectal es el más apropiado para la proctitis ulcerosa activa. Los supositorios alcanzan el recto proximal, llegando hasta 15 a 20 cm del ano y los enemas pueden llegar más allá del ángulo esplénico.
Para el tratamiento de la proctitis ulcerosa activa se recomienda la utilización de supositorios de 5-ASA (mesalazina) como tratamiento de primera línea por su efectividad y pocos efectos colaterales.
En México se cuenta con la presentación de supositorios de 5-ASA de 500 mg y de 1 g, se recomienda la dosis de 1 g al día durante un mes. La administración de 1 a 4 g al día en supositorios o en espuma, es habitualmente la más utilizada. Después del mes, se puede ir disminuyendo la dosis a 1 g en días alternados. Del 40 al 80% de los pacientes tendrán una resolución completa de los síntomas en un término de 4 a 8 semanas de tratamiento.
Algunos pacientes refieren que 5-ASA en espuma es una presentación más fácil de retener y más cómoda, en comparación con el enema líquido. El enema gel de 5-ASA es igualmente efectivo y bien tolerado.
Los pacientes que no responden o no toleran el tratamiento con 5-ASA, tienen dos opciones: 5-ASA vía oral y esteroides vía rectal. Para el tratamiento con 5-ASA vía oral se recomienda una dosis diaria de mesalazina de 2.5 a 5 g al día. Es importante mencionar que no debe suspenderse el tratamiento vía rectal con 5-ASA, debido a que el empleo vía oral de este producto no es tan efectivo si se administra solo, en comparación con la vía rectal. Dentro de las probables causas de la poca efectividad de las preparaciones vía oral del 5-ASA para el tratamiento de la proctitis, destaca la estasis colónica proximal y el tránsito rápido a través de la zona colónica distal inflamada; estas circunstancias limitan el tiempo de exposición del producto vía oral en esta zona. La combinación de 5-ASA vías oral y rectal ofrece los mejores resultados, probablemente debido a un efecto dosis-respuesta y un tiempo de contacto significativamente mayor del producto que con la mucosa colónica distal.
En caso de decidir iniciar con corticoesteroides vía rectal, éstos pueden aplicarse solos o en conjunto con 5-ASA. Se utilizan las presentaciones en supositorios, enema 2 ó 3 o espuma. En México se cuenta con budesonida de 3 mg.
En pacientes que no responden al tratamiento con compuestos de 5-ASA y/o glucocorticoides tópicos (rectales), o con síntomas particularmente difíciles de controlar, están indicados los esteroides vía oral. La prednisona vía oral debe iniciarse con dosis de 40 a 60 mg/día hasta lograr una mejoría clínica; posteriormente se reducirá de 5 a 10 mg por semana, hasta alcanzar una dosis de 20 mg; a partir de este momento, se disminuye a razón de 2.5 mg/semana.
Otra opción es la budesonida. Es un corticoesteroide que se metaboliza rápidamente en el hígado, por lo que se reducen los efectos secundarios relacionados con este tipo de fármacos. Actualmente hay tres formulaciones de budesonida: dos cápsulas estándar, ambas diseñadas para liberar el fármaco en la parte exterior del intestino delgado y la parte derecha del colon; la cápsula más nueva, Budesonida-MMX®, diseñada para liberar el fármaco a lo largo de todo el colon. La dosis de 9 mg/día por 2 ó 3 meses es eficaz en la mayoría de los enfermos.
Otras alternativas en el paciente refractario al tratamiento son los enemas de ácidos grasos de cadena corta, enemas o parches de nicotina, supositorios de acetarsol, lidocaína tópica y enemas de factor de crecimiento epidermoide.
Si aun con lo anterior no hay una mejoría clínica, el paciente debe hospitalizarse e iniciar esteroides intravenosos. Otra opción es la utilización de azatioprina a 1.5 a 2.5 mg/kg; si continuara el paciente sin mejoría está indicada la colectomía.
El paciente debe tomar o aplicarse el menor número de tabletas, supositorios o enemas que lo mantengan libre de actividad. Algunos autores consideran que es necesario comunicarse con el paciente de 1 a 2 semanas después de iniciado el tratamiento, para conocer si ha sido adecuadamente tolerado y si hay un buen apego al mismo. El seguimiento clínico en consulta debe hacerse cada 4 a 8 semanas para corroborar la remisión de la enfermedad.
La administración de 5-ASA rectal es el tratamiento ideal para el mantenimiento de la proctitis ulcerosa. En la experiencia de algunos autores, en los pacientes que responden adecuadamente durante un mes de tratamiento de mesalazina diario, se puede iniciar la reducción de la dosis a días alternos.
Las guías de tratamiento de la Sociedad Británica de Gastroenterología, la Sociedad Alemana del Tracto Digestivo y Trastornos Metabólicos y de la Asociación Mexicana de Gastroenterología, sugieren una dosis de mantenimiento de mesalazina de 1 a 2 g/día, además de la aplicación rectal. Consideran las mismas sociedades, que es razonable suspender el tratamiento en los pacientes con enfermedad distal, que han estado en remisión por lo menos dos años. Además, el riesgo de cáncer colorrectal parece disminuir si se combina la terapia de mantenimiento.
Es importante aclarar que este término no es empleado literalmente en la clasificación de Montreal para extensión de la enfermedad. Sin embargo, se hace mención de la misma por el gran número de reportes en estudios endoscópicos que señalan a esta zona específica de la enfermedad. La mayoría de los autores considera que una proctosigmoiditis debe de tratarse de la misma manera que una colitis izquierda. Para la inducción de remisión y mantenimiento, el tratamiento vía rectal de 5-ASA o corticoesteroides es lo más apropiado para la proctosigmoiditis y la colitis ulcerosa izquierda activa. Los enemas, espumas y geles, por la distancia que alcanzan en el colon durante su aplicación, serán los vehículos apropiados.
La colitis izquierda activa (recto, sigmoides y colon descendente), debe tratarse con 5-ASA vía rectal. La administración de corticoesteroides vía rectal es una alternativa adecuada para los pacientes que no toleran o no tienen respuesta al 5-ASA. En los pacientes sin una respuesta adecuada al 5-ASA vía rectal o esteroides vía rectal se tienen dos opciones: 5-ASA vía rectal más corticoesteroides vía rectal o una combinación de 5-ASA vía oral y rectal. Los corticoesteroides orales se reservan para los pacientes que no responden a la administración rectal de 5-ASA y/o corticoesteroides o 5-ASA vía oral. Los enemas de mesalazina se deben administrar por la noche, y el tiempo de respuesta clínica puede tomar de 2 a 4 semanas. En caso de no haber una respuesta satisfactoria a las 2 semanas, se debe iniciar con enemas de hidrocortisona o de budesonida. En estos casos, la administración conjunta de 5-ASA vía oral y rectal es una terapéutica más efectiva que el utilizar sólo una vía de administración.
Una vez que se han empleado todas las combinaciones antes mencionadas sin una respuesta adecuada, se debe iniciar el tratamiento con corticoesteroides vía oral. La mayor parte de los pacientes responden adecuadamente con la utilización de 40 mg vía oral de prednisona (o su equivalente). Esta dosis casi siempre se mantiene por 1 a 2 semanas hasta alcanzar una respuesta clínica satisfactoria; posteriormente se inicia la reducción de la dosis del corticoesteroide; en el caso de la prednisona se reduce de 5 a 10 mg por semana. Es importante que la administración vía oral y rectal de 5-ASA se mantenga en conjunto con los corticoesteroides, con la intención de mantener la remisión de la enfermedad. La utilización de antibióticos en estos casos no tiene un sustento adecuado; sin embargo, se ha informado cierta efectividad en algunos pacientes. Su utilización puede ser una opción en algunos casos que no responden con 5-ASA o corticoesteroides.
La administración de 5-ASA rectal es efectiva en el mantenimiento de la remisión en la mayoría de los pacientes. Sin embargo, aquellos casos en los cuales se ha alcanzado una respuesta adecuada con 5-ASA vía oral y rectal, deberá continuarse con el mismo manejo. Por otra parte, la administración vía oral de 5-ASA es una alternativa eficaz a la administración vía rectal de este medicamento para mantener la remisión.
Los inmunomoduladores como la azatioprina o 6-mercaptopurina, e incluso el infliximab, pueden requerirse para el mantenimiento de los pacientes dependientes de esteroides. Los pacientes que responden a enema de mesalazina como monoterapia pueden mantener la remisión con dosis desde una vez a la semana hasta su administración diaria.
Aun en los pacientes con colitis extensa, se recomienda iniciar con 5-ASA. La combinación vía rectal y oral mejora la respuesta inicial. Una dosis vía oral mayor de 4 a 4.8 g es lo apropiado para iniciar el tratamiento de los pacientes con colitis ulcerosa extensa leve y moderada. En los pacientes en quienes no hay una mejoría después de 2 semanas de haber iniciado el tratamiento combinado, deberá agregarse terapia con corticoesteroides orales. La 6-mercaptopurina y la azatioprina son efectivas para los pacientes que no responden a la prednisona, pero que no se encuentran con sintomatología tan severa que requiera terapia intravenosa. Hay estudios que muestran a la nicotina en parches como una alternativa efectiva para alcanzar la remisión, en dosis de 15 a 25 mg diarios. Para el mantenimiento de la remisión se deberá continuar con el esquema habitual de 5-ASA vía oral y rectal (Cuadro 14).
| Cuadro 14. Tratamiento para la inducción y mantenimiento de la colitis ulcerosa crónica idiopática (CUCI) | |||
| Droga | Dosis | Indicación | Vía de administración |
| Balsalazida | 2.5 a 6.75 g/día | Inducción y mantenimiento | Oral |
| Olsalazina | 1.5 a 3 g/día | Inducción y mantenimiento | Oral |
| Sulfasalazina | 2 a 4.5 g/día | Inducción y mantenimiento | Oral |
| Mesalazina | 2.5 a 5 g/día | Inducción y mantenimiento | Oral y rectal |
| Prednisolona | 40 mg/día | Inducción | Oral |
| Prednisona | 0.5 a 1 mg/kg/día | Inducción | Oral |
| Hidrocortisona | 400 mg/día | Inducción | Intravenosa |
| Metilprednisolona | 60 g/día | Inducción | Intravenosa |
| Budesonida | 6 a 9 mg/día | Inducción | Oral y rectal |
| Azatioprina | 1.5 a 2.5 mg/kg/día | Mantenimiento | Oral |
| 6-Mercaptopurina | 0.75 a 1.5 mg/kg/día | Mantenimiento | Oral |
| Ciclosporina A | 2 a 4 mg/kg/día | Inducción | Oral e intravenosa |
| Metotrexato | 15 a 25 mg/semana | Inducción y mantenimiento | Oral e intramuscular |
| Infliximab | 5 mg/kg/0, 2, 6 posterior c/8 semanas | Inducción y mantenimiento | Intravenosa |
| Adalimumab | 160/80/40 mg/kg/quincenal | Inducción y mantenimiento | Subcutánea |
Otros fármacos utilizados en la colitis leve y moderada son los derivados del tiazol, como tetomilast (OPC-6535, Otsuka Maryland Research Institute, Rockville, MD), en estudios fase III para remisión y mantenimiento. Los inhibidores moleculares selectivos de la adhesión leucocitaria son otra opción en estudio para remisión de la enfermedad. Un ejemplo es el MLN02 (Millenium Pharmaceuticlas, Cambridge, MA). Otros medicamentos de esta clase utilizados en CUC son: abatacept, alicarforsen y natalizumab. Terapia dirigida contra células T, como el vizilizumab y el basiliximab son utilizados en pacientes resistentes a corticoesteroides. El dactalizumab es un anticuerpo monoclonal recombinante humano del tipo Ig G1, que basa su efectividad a la alta afinidad a los receptores de la IL-2.
El golimumab es un anticuerpo monoclonal anti-TNF-α de origen humano en pacientes con actividad moderada a grave de administración subcutánea. El vedolizumab es un anticuerpo monoclonal humanizado específico cuyo blanco es la integrina α4β7 que interactúa con la molécula de adhesión MAdCAM-1. El etrolizumab es un anticuerpo monoclonal humanizado específico cuyo blanco es la subunidad β7 de las integrinas heterodiméricas α4β7 y αEβ7. Otras sustancias han probado eficacia en el tratamiento de los pacientes portadores de CUCI como tofacitinib, tralokinumab, eldelumab, ISIS 2302, entre otros.
Las manifestaciones extraintestinales se presentan en el 25% de los pacientes con enfermedad inflamatoria intestinal y se dividen en tres clases distintas:
Clase I. Enfermedades mediadas por compromiso inmunológico. Aquí hay dos grupos: el primero incluye aquellas manifestaciones reactivas asociadas con la actividad de la enfermedad inflamatoria intestinal y, por lo tanto, reflejan un mecanismo patogénico (artritis, eritema nodoso, pioderma gangrenoso, estomatitis aftosa, iritis y uveítis). El segundo grupo incluye enfermedades autoinmunes independientes que sólo reflejan una mayor susceptibilidad a la autoinmunidad. Éstas no se consideran específicas de la enfermedad inflamatoria intestinal (espondilitis anquilosante, cirrosis biliar primaria, alopecia areata y tiroiditis autoinmune).
Clase II. Complicaciones directamente relacionadas con enfermedad inflamatoria intestinal crónica, como la uropatía obstructiva, malabsorción, nefrolitiasis y colelitiasis.
Clase III. Manifestaciones que no están dentro de las dos anteriores, como la amiloidosis.
De forma general, la CUCI no tiene efecto alguno sobre la fertilidad ni sobre la evolución del embarazo. Por otra parte, la gestación no afecta a la evolución de la CUCI. Sin embargo, la evolución de la CUCI y la gestación se correlacionan con la actividad de la enfermedad en el momento de la concepción, de forma que la existencia de brote de actividad en este momento se ha asociado a un mayor riesgo de aborto y a una peor respuesta al tratamiento médico de la CUCI.
La sulfasalazina y la mesalazina pueden utilizarse de forma segura durante la gestación. La sulfasalzina interfiere en la absorción de folatos (de gran importancia en la formación del tubo neural del feto), por lo que es recomendable administrar 2 mg/día de ácido fólico durante la gestación cuando se prescriba este fármaco. Existen dudas acerca de la nefrotoxicidad fetal por parte de la mesalazina, por lo que es recomendable no exceder los 2 g/día durante el embarazo.
Los esteroides no han mostrado efectos deletéreos sobre el embarazo o el feto humanos, por lo que pueden emplearse con seguridad, aunque inicialmente se ha demostrado su teratogenicidad en animales.
La AZA ha demostrado su teratogenia en animales, pero no en humanos; a pesar de haberse descrito más de 1 000 gestaciones sin teratogenia, sí se han descrito casos aislados de hipoplasia tímica, linfopenia e hipogammaglobulinemia. En caso de gestación durante el tratamiento con AZA es recomendable revalorar detalladamente la indicación del tratamiento y, en caso necesario, seguir con el tratamiento siempre previa información detallada al paciente.
CyA no ha demostrado tener efectos teratogénicos en animales ni en humanos; sin embargo, alrededor del 50% de los recién nacidos de madres bajo tratamiento son prematuros o presentan bajo peso al nacer. Por otra parte, la CyA pasa en concentraciones importantes a la leche materna, por lo que está claramente contraindicada durante la lactancia.
El metronidazol y el ciprofloxacino, fármacos de uso frecuente en la CUCI, deben evitarse en el embarazo y la lactancia.
El tratamiento de la CUCI en edad pediátrica no difiere del adulto. Únicamente debe tenerse en cuenta el efecto del uso prolongado de corticoesteroides y de la desnutrición sobre el crecimiento, por lo que es de gran trascendencia prevenirlos. Esto puede significar en algunas situaciones la indicación de colectomía de forma más precoz que en el adulto, especialmente cuando la CUCI se asocia a retraso del crecimiento.
La respuesta al tratamiento médico de la CUCI en general es satisfactoria. Con el advenimiento de nuevos medicamentos, el éxito en la remisión en CUCI leve es mayor del 90% y en los casos de enfermedad moderada alcanza hasta el 77%. En los pacientes graves, la respuesta al tratamiento es mucho menor. Actualmente, hasta el 45% de los pacientes portadores de esta enfermedad requieren cirugía en algún momento de su vida. Existen dos modalidades para el tratamiento quirúrgico: 1) cirugía urgente y 2) cirugía electiva.
Para los pacientes con colitis grave, más de 5 días de evolución sin mejoría y en aquellos que ya presentan una complicación como megacolon tóxico, hemorragia masiva, obstrucción o perforación, la colectomía subtotal con ileostomía terminal es la mejor alternativa. Se requiere de un abordaje multidisciplinario que involucra al gastroenterólogo, endoscopista, radiólogo, nutriólogo, terapeuta enterostomal y al cirujano. Una vez que las condiciones del paciente se estabilizan, se procede a realizar la proctectomía y la creación de un reservorio ileal.
Sin embargo, hoy por hoy la indicación más frecuente para el tratamiento quirúrgico es la falta de respuesta al tratamiento médico.
La colitis aguda y grave definida de acuerdo a los criterios de Truelove y Witts se caracterizan por 6 evacuaciones diarreicas o más en 24 h, acompañadas con sangre, además de signos de toxicidad sistémica, como taquicardia de más de 90x’, fiebre mayor a 37.8 °C, hemoglobina menor a 10.5 g/dL y una velocidad de sedimentación globular mayor a 30 mm/h.
Estos pacientes deben ser hospitalizados e iniciar el tratamiento médico; alrededor del 40% requerirá cirugía de urgencia; el arte de determinar el momento idóneo no es una decisión fácil y recae en el juicio clínico del gastroenterólogo y el cirujano.
Es muy importante recalcar que esta decisión debe tomarse de manera temprana; el deterioro del paciente, no obstante un tratamiento médico adecuado, debe ser indicación para cirugía.
El manejo cotidiano es un curso de tratamiento médico intensivo por 5 a 7 días seguido de una colectomía en aquellos pacientes que no mejoran.
Los indicadores clínicos que al ingreso señalan mayor probabilidad de cirugía incluyen: más de diez evacuaciones con sangre en 24 h, albúmina y hematocrito bajos y descenso del 10% o más de la masa corporal. Los ataques recurrentes y graves son también una indicación de que la terapia de mantenimiento ha fallado y por tanto es preferible decidir una cirugía temprana. Después del inicio de la enfermedad la posibilidad de cirugía es mayor durante el primer año.
Al internar al paciente es muy importante vigilar su evolución muy cercanamente para determinar si existe o no mejoría. La posibilidad de que un paciente requiera colectomía en ese mismo ingreso es del 85% si al tercer día de internamiento continúa con 8 o más evacuaciones disenteriformes. Por esto es que la bitácora de sus evacuaciones debe ser muy cuidadosa. Si al día tres hay entre 3 a 8 evacuaciones con sangre y la proteína C reactiva es mayor a 45 mg/L, fiebre de 38 °C, esta posibilidad es del 75%.
El paciente grave debe examinarse dos a tres veces al día, con especial atención a la presencia de distensión abdominal, signo que debe hacer pensar en la posibilidad de un megacolon tóxico; las radiografías de abdomen permitirán medir el diámetro del colon y buscar la presencia de gas intramural, signo inminente de perforación. El desarrollo de rigidez en la pared abdominal sugiere peritonitis local o generalizada y en estos casos es necesaria cirugía inmediata.
La perforación puede ser silenciosa; son pacientes que están recibiendo grandes dosis de esteroides o inmunomoduladores, etcétera, y a veces la perforación sólo se evidencia en la placa simple de abdomen; el no sospechar este diagnóstico, ni actuar oportunamente empeora el ya sombrío pronóstico del paciente (Figura 23).
Figura 23
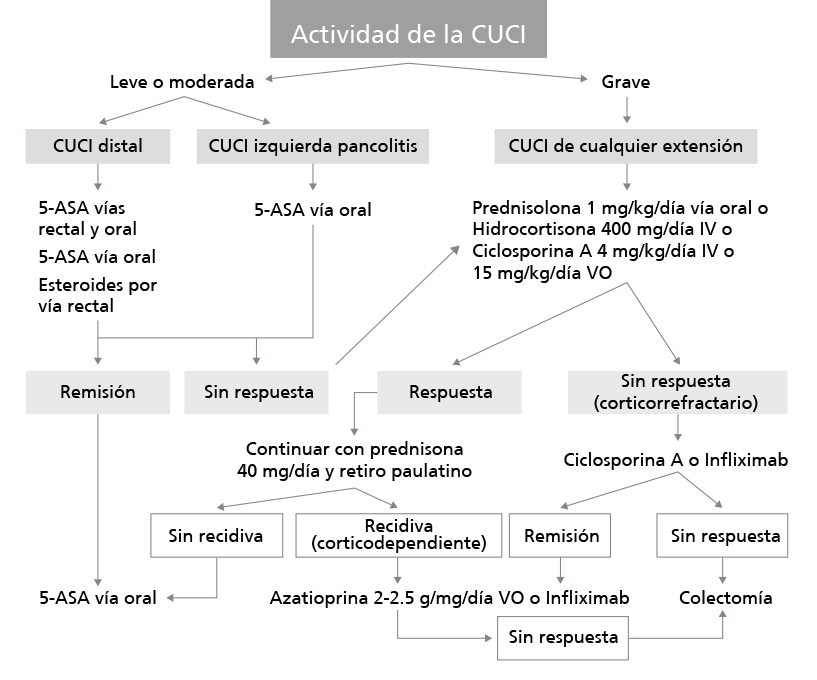
Algoritmo en el manejo de la colitis ulcerosa crónica idiopática.
En casos graves de urgencia, el procedimiento quirúrgico debe ser colectomía con ileostomía, conservando el muñón rectal. El Consenso Europeo recomienda esta técnica además, cuando el paciente ha tomado 20 mg o más de prednisolona por más de 6 semanas.
La mayoría de los pacientes que requieren cirugía son aquellos que presentan una colitis extensa, enfermedad sistémica y síntomas graves. Estos pacientes tienen mayor riesgo de desarrollar episodios de colitis aguda y grave, y de presentar cambios malignos y manifestaciones extraintestinales. Esporádicamente un paciente con enfermedad distal puede requerir tratamiento quirúrgico, casi siempre por síntomas locales graves.
En pacientes con enfermedad intratable, cuando no se controlan los síntomas con medicamentos o hay una respuesta inadecuada a los mismos o aparecen efectos adversos o complicaciones por la utilización de estos fármacos, está indicado un procedimiento electivo; otras indicaciones de la cirugía son el retraso en el crecimiento en los niños, la presencia de lesiones asociadas a displasia no adenomatosa (DALM), displasia de alto grado, displasia de bajo grado asociada a una estenosis, profilaxis para cáncer, hemorragia recurrente, manifestaciones extraintestinales y carcinoma; en algunos casos se ha sugerido a solicitud del paciente y falta de apego al tratamiento por contar con seguridad social y recursos económicos.
La proctocolectomía restaurativa con reservorio ileal ha sido propuesta en todo el mundo como el estándar quirúrgico; sin embargo, es una cirugía que conlleva riesgos como la “pouchitis”, que representa la complicación más frecuente a largo plazo. Algunas de las contraindicaciones para realizar una cirugía restaurativa son: 1) enfermedad de Crohn; 2) lesión de los esfínteres anales; 3) enfermedad anoperineal previa; 4) comorbilidades. Una edad mayor de 60 años se asocia a un resultado poco satisfactorio de la cirugía. En cuanto a la configuración del reservorio ileal, la forma en “J” propuesta por Utsunomiya es la más utilizada; otras opciones son en “W” o en “S”. Algunas sugieren realizar el procedimiento restaurativo en un solo tiempo, esto es, sin una ileostomía en asa de protección. Sin embargo, es preferible construirla y cerrarla después de 3 a 6 meses.
La proctocolectomía con ileostomía terminal tipo Brooke sigue siendo el procedimiento con el cual se comparan todos los realizados; se indica en aquellos pacientes con esfínteres anales no funcionales, pacientes de alto riesgo y en quienes no desean un reservorio ileal. La ileostomía continente tipo Kock, casi en desuso en estos días, se ha asociado a complicaciones en más del 50% de los casos por inadecuado funcionamiento u obstrucción a nivel de la válvula ileal continente. La colectomía subtotal con ileostomía se ha empleado como tratamiento paliativo cuando se encuentra un cáncer de recto avanzado; la colectomía subtotal con ileoproctostomía sólo se recomienda en casos de colitis indeterminada con mínima afección del recto y del ano, así como en pacientes con cáncer colorrectal con metástasis.
En gran medida la cirugía depende del deseo del paciente por lo cual es esencial darle una información detallada de la morbilidad, función, complicaciones tempranas y tardías y probable duración operatoria de cada una de las opciones quirúrgicas. Es indudable el valor y la conveniencia de contar con un terapeuta enterostomal y sería ideal que el enfermo y la familia se integren a un grupo de apoyo de pacientes ostomizados.
Aunque está claramente establecido que en la CUCI el riesgo de desarrollar cáncer colorrectal (CCR) se encuentra aumentado, la magnitud de este riesgo no se ha definido en detalle. El riesgo acumulado de CCR en pacientes con pancolitis se estima en aproximadamente el 30% a los 30 años, con una incidencia del 0.5 al 1% anual. Este riesgo se ve incrementado respecto a la población general a partir de los 8 años de evolución de la CUCI y también en función de la extensión de ésta, siendo máximo en la pancolitis y normal, respecto a la población general, en la proctitis. Probablemente existen otros factores que influyen en el riesgo de CCR además de la duración y extensión de la enfermedad, algunos de los cuales (como la asociación a colangitis esclerosante primaria) ya han quedado demostrados. Se desconoce por el momento si el uso de inmunosupresores ejerce algún papel sobre este riesgo.
Por todo ello, se recomienda seguir estrategias de vigilancia encaminadas a la detección de focos de displasia o de CCR en estadios tempranos, mediante la realización de colonoscopias con toma de biopsias seriadas múltiples a distintos niveles del colon. Aunque no disponemos de estudios comparativos entre colectomía profiláctica y vigilancia endoscópica, y el único análisis de decisión disponible no sugiere un gran beneficio de los programas de seguimiento, la mayoría de los centros de referencia aplican una política de seguimiento.