Figura 10
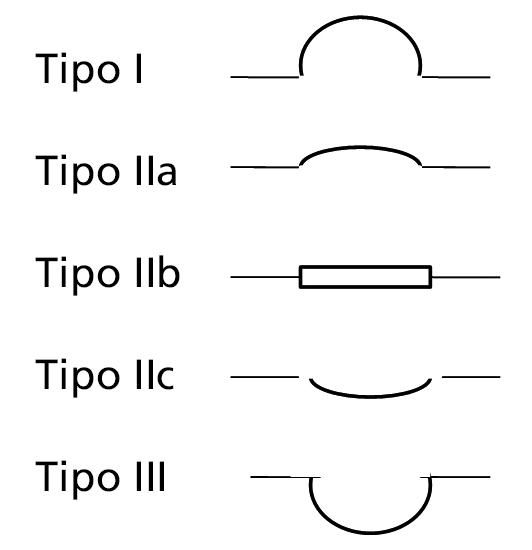
Clasificación de cáncer gástrico incipiente.
Coordinador: Dr. Juan Miguel Abdo Francis
Cáncer gástrico
Dr. Antonio de la Torre Bravo
El cáncer gástrico es la neoplasia maligna más frecuente del aparato digestivo, ocupa el cuarto lugar en morbilidad y el quinto en mortalidad entre todos los tumores malignos en México. Predomina en el sexo masculino con una relación de 2:1 sobre el femenino (Cuadros 8 y 9).1,2 A nivel mundial, México se considera entre los países de riesgo bajo por tener una tasa de incidencia menor a 10 x 100 000 habitantes calculada en 5 x 100 000. En los países de altos ingresos se ha observado una tendencia a la disminución, la cual no se ha demostrado en nuestro país. En una revisión personal de los tres últimos años de los que se tiene información, la tasa se mantiene en la misma cifra. Los estados con mayor mortalidad son Chiapas con tasa de 6.4, Ciudad de México 4.5 y Estado de México 2.5.1,2 En cambio, el carcinoma de la unión esofagogástrica tiene un ascenso alarmante en los últimos 30 años.
| Cuadro 8. Morbilidad de los tumores malignos más frecuentes en México, 2002 | |
| Localización | Número |
| Glándula mamaria | 12 169 |
| Cuello uterino | 9 812 |
| Próstata | 6 365 |
| Estómago | 3 464 |
| Cuadro 9. Mortalidad de los tumores malignos más frecuentes en México, 2002 | |
| Localización | Número |
| Cáncer de pulmón | 6 571 |
| Estómago | 5 136 |
| Cuello uterino | 4 330 |
| Próstata | 4 231 |
Existe un factor hereditario en una minoría que se sospecha cuando hay dos casos en menores de 50 años en la misma familia o tres a cualquier edad. En la mitad de estos pacientes hay una mutación somática del gen E-cadherina. Este factor se observa en 2 a 3% de todos los carcinomas gástricos.3
Se han propuesto factores de la dieta como la ingesta de alimentos con conservadores, alimentos ahumados y secados con sal. Se menciona un factor protector de la dieta la ingesta de suplementos de betacaroteno, selenio y alfatocoferol. Otros factores con papel carcinogénico son el grupo sanguíneo A, alimentos crudos o poco cocidos, los nitritos y la carencia de refrigeración. Helicobacter pylori ha sido considerado carcinógeno tipo I; sin embargo, no hay correlación entre la frecuencia de ambas entidades por lo que es posible la existencia de factores propios del germen y propios del huésped para el efecto carcinógeno, principalmente por la virulencia del primero a través de sus enzimas VacA y CagA. Uno de los primeros estudios que apoyaron la hipótesis de H. pylori como carcinógeno consistió en inocular el germen por vía oral en 55 gerbos y al final de 62 semanas 10% había desarrollado adenocarcinoma vs. 0 en 30 controles no infectados.4
La secuencia hipotética de la evolución de la mucosa a adenocarcinoma propuesta por Pelayo Correa es: mucosa normal – infección por H. pylori – gastritis crónica superficial – gastritis crónica atrófica – gastritis crónica con metaplasia intestinal – carcinoma gástrico.5
La neoplasia que se presenta con mayor frecuencia en el estómago es el adenocarcinoma, seguida del linfoma gástrico primario, leiomiosarcoma, carcinoide y sarcoma de Kaposi. El carcinoma ocupa alrededor del 94% de los tumores gástricos. La Clasificación de Laurent6 consiste en dos tipos: uno, denominado difuso, caracterizado por células malignas no cohesivas y otro identificado por el acomodo de las células formando glándulas y es precedido por metaplasia intestinal. El primero se presenta en personas de edad relativamente más joven y se localiza en el cuerpo y fondo; en cambio, el segundo afecta personas de edad avanzada, se sitúa en el antro y es menos agresivo que el anterior.
El cáncer gástrico se origina en la mucosa y tiende a extenderse superficialmente, aunque avanza predominante en profundidad a la submucosa, a la capa muscular y a la serosa. En esa etapa envía metástasis a los ganglios perigástricos. Al igual que se extiende al resto de la mucosa, invade a los órganos vecinos como el colon transverso, el páncreas, el diafragma, los grandes vasos retroperitoneales, el epiplón y, progresivamente, los ganglios periesofágicos, los del tronco celiaco y a los del hilio esplénico. Por vía transcelómica avanza al peritoneo y por hematógena al hígado y a los pulmones. A partir de este momento puede dar metástasis a cualquier sitio del cuerpo.
La edad de aparición de los síntomas es por arriba de los 45 años con una media situada en el séptimo decenio de la vida, aunque hay casos informados desde el segundo decenio, pero son rarezas. Es más frecuente en hombres en relación de 2:1. El síntoma predominante es molestia o dolor epigástrico que no cede con los alimentos, sino por lo contrario, aumenta con los mismos. Otros síntomas son náusea, hemorragia, anemia y pérdida de peso. Cuando hay disfagia es debida a infiltración de la unión esofagogástrica y cuando hay vómito, lo es por obstrucción pilórica. A la exploración es posible identificar una masa en el epigastrio, hepatomegalia y adenopatías supraclavicular o axilar izquierdas. Esporádicamente se encuentra una masa pélvica por metástasis al ovario denominado tumor de Krukenberg.
Una cualidad de esta enfermedad, similar a la de otras neoplasias es que el diagnóstico oportuno permite un mejor pronóstico, incluso la curación. En Japón, por su alta prevalencia de cáncer gástrico, se justifica la detección en personas asintomáticas. El resultado es la identificación de tumores confinados a la mucosa y a la submucosa, a lo que se denomina carcinoma gástrico incipiente, y cuyo pronóstico a cinco años es superior al 85%. Un hallazgo agregado fue que, a posteriori, se descubrió que parte de sus casos “asintomáticos” sí tenían algún síntoma, como molestia o dolor epigástrico. Estudios posteriores en el seguimiento de pacientes con carcinoma incipiente del estómago han demostrado su permanencia en esa etapa durante 39 meses antes de alcanzar la etapa de neoplasia avanzada.
Ese hallazgo obligó a los países occidentales a no tomar a la ligera los síntomas gástricos en pacientes mayores de 45 años. Es necesario, en estos enfermos, identificar la causa del dolor antes de etiquetarlos como enfermedad acidopéptica y tratarlos en forma empírica con antiácidos o analgésicos. La mayoría de los pacientes con cáncer gástrico avanzado refieren que al inicio de su enfermedad o no consultaron a un médico y utilizaron automedicación o consultaron a un profesional o a varios y sólo recibieron medicamentos sintomáticos en forma repetitiva y a ninguno se le ocurrió una exploración endoscópica.
Específicamente, el diagnóstico del cáncer gástrico incipiente se logra a través de la endoscopia con biopsia.7,8 La serie gastroduodenal con doble contraste también tiene utilidad cuando no se dispone de la anterior porque su sensibilidad es baja. En ambos estudios se requiere el conocimiento de la imagen y de su clasificación (Figura 10); el tipo más frecuente es el tipo IIc que es deprimido. En la práctica muy especializada, el carcinoma gástrico incipiente tipos I y II pueden ser resecados endoscópicamente inyectando líquido en la submucosa para elevarlos y con un cuchillo y corriente eléctrica cortar el contorno y su base, mencionando esto como un ejemplo de la simplicidad de tratamiento cuando el diagnóstico es temprano.
Figura 10

Clasificación de cáncer gástrico incipiente.
La sospecha clínica debe ser seguida de procedimientos de gabinete para confirmar o descartar un tumor maligno en el estómago. El procedimiento tradicional ha sido el estudio baritado del tubo digestivo alto con doble contraste, bario y aire, pero sólo es útil cuando el síntoma predominante es la disfagia o cuando se sospecha un tumor muy avanzado, pero prácticamente se ha reservado para sitios donde no se dispone de la endoscopia.9 El procedimiento de elección es la endoscopia gracias a su capacidad de identificar todas las lesiones, incluso las más pequeñas, valorar la localización, la forma (Figuras 11, 12, 13, y 14) y la extensión y lograr el enorme beneficio de las biopsias que tienen una especificidad cercana a 100%.
Figura 11
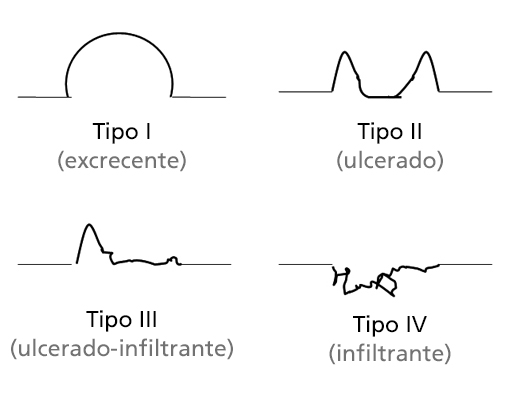
Clasificación del cáncer gástrico avanzado.
Figura 12
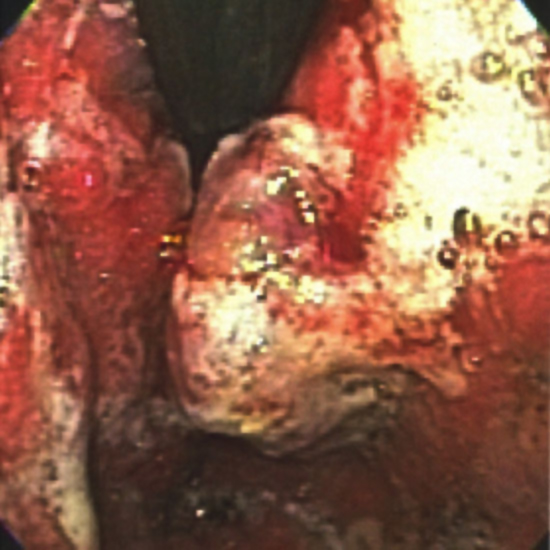
Cáncer gástrico Borrmann tipo I.
Figura 13
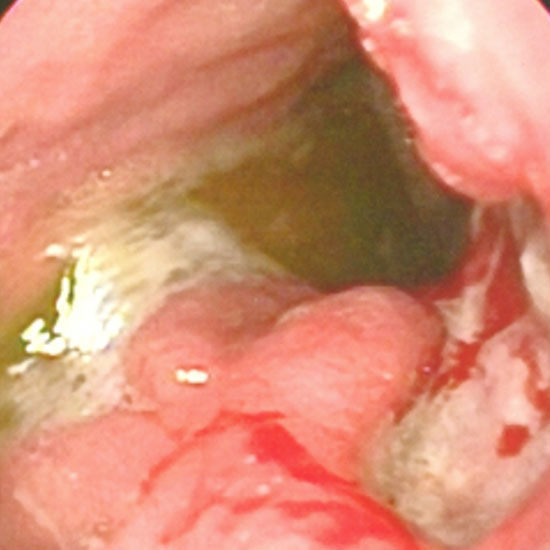
Cáncer gástrico Borrmann tipo II.
Figura 14
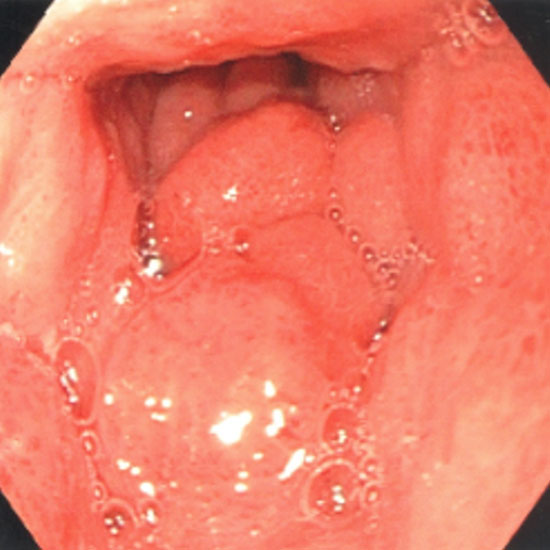
Cáncer gástrico Borrmann tipo IV.
Una vez logrado el diagnóstico del tumor primario el resto de los estudios tienen el objetivo de determinar la extensión. Primero, el ultrasonido endoscópico explora la profundidad del tumor en la pared y la posible invasión a los ganglios linfáticos perigástricos y algunos de las cadenas secundarias, así como la invasión a órganos vecinos. En ausencia del ultrasonido endoscópico o en conjunto con éste, la tomografía computada también valora la extensión del tumor a órganos vecinos y metástasis al hígado, por ejemplo. La telerradiografía de tórax aporta información de la salud o enfermedad arriba del diafragma. La biometría hemática mide la anemia, generalmente presente, y las pruebas de funcionamiento hepático exploran la posibilidad de metástasis hepáticas.
Al final, se logra un diagnóstico muy completo lo cual permite una clasificación conocida como TNM; la T expresa el tamaño de tumor, la N gradúa las posibles metástasis ganglionares y la M afirma o descarta metástasis a distancia. Reservamos la clasificación completa para el especialista, pero con brevedad se ilustra la sistematización que rodea al diagnóstico para determinar el tratamiento que más conviene a cada paciente.
La detección del cáncer gástrico incipiente y la de los tumores en estadios tempranos es baja, del 10 al 20% de los casos estudiados. Más del 80% de las neoplasias son avanzadas y la posibilidad de resección curativa es baja, con una supervivencia del 10 al 15% a cinco años. El médico de primer contacto o el no especialista en Oncología, debe referir al paciente a un centro oncológico donde se concentran los recursos necesarios para la adecuada atención del paciente con cáncer gástrico: cirugía, quimioterapia y radioterapia.
El tratamiento fundamental para el cáncer gástrico es la cirugía. La selección del tipo de intervención quirúrgica depende de la localización del tumor: cuando se sitúa en el antro gástrico se prefiere la gastrectomía distal o subtotal con amplio margen proximal y anastomosis gastroyeyunal. La localización en el cuerpo y el fondo obliga a la gastrectomía total y en casos excepcionales, la gastrectomía subtotal proximal. La infiltración a la unión esofagogástrica obliga a la esofagectomía distal o total, con ascenso gástrico residual o el uso de un segmento colónico para restablecer la continuidad. La cirugía oncológica cuida la resección de las diversas cadenas ganglionares involucradas en la misma pieza. Según el grado de avance tumoral se utiliza quimioterapia peritumoral sola o asociada a radioterapia. En los casos muy avanzados puede hacerse la gastrectomía paliativa, la gastroyeyunoanastomosis en tumores proximales o sólo quimioterapia. Esta breve descripción establece que el tratamiento es complejo y se intenta desalentar la audacia del cirujano general distante de los tratamientos multidisciplinarios.
El pronóstico está en relación inversamente proporcional al grado de avance tumoral y se ubica alrededor del 7 al 10%.
Si el autor quisiera rescatar un mensaje de todo lo dicho, lo resumiría en la importancia del diagnóstico oportuno. Pasar por alto los síntomas de alarma: anemia, hemorragia, pérdida de peso, disfagia y vómito persistente es negligencia. El estudio a fondo del malestar o el dolor epigástrico en mayores de 45 años es sagacidad clínica.