Figura 13
Distribución histórica de casos de tuberculosis meníngea en niños menores de 5 años y millones de dosis de BCG aplicadas. México, 1990–2010. Fuente: DGE/CENSIA/Secretaría de Salud.
Coordinador: Dr. Miguel Ángel Rodríguez Weber
vacunas para el control y prevenciÓn de enfermedades en MÉxico
Dr. Miguel Ángel Rodríguez Weber, Dra. Samia Gaffare Aranda, Dr. Eduardo Arias De la Garza
En la actualidad una de las mejores formas de prevenir y controlar las enfermedades transmisibles en la población pediátrica es el adecuado empleo de vacunas. Su relación “costo-efectividad” y “costo-beneficio” han quedado demostradas de manera contundente tanto a nivel nacional como a nivel internacional.
Varios padecimientos que en otras épocas originaban devastación en la población debido a su elevada morbimortalidad y al elevado costo para su atención, hoy han podido controlarse razonablemente e incluso se ha logrado su erradicación en algunos países, en regiones continentales y a nivel mundial. El ejemplo más evidente lo representa la viruela que la OMS (Organización Mundial de la Salud) considera erradicada a nivel mundial.
Pueden existir ideas equivocadas en la comunidad y en el personal de salud respecto de algunas situaciones específicas por las que consideran que no se deben vacunar a niños apegándose al Programa Nacional de Vacunación; algunas de ellas son: niños prematuros, niños con malformaciones congénitas, antecedente de hospitalización prolongada o de intervenciones quirúrgicas, displasia broncopulmonar, deficiencias neurológicas. Ninguna de ellas es una contraindicación médica para que reciban su esquema de vacunación normal.
En México se inició la vacunación en 1926 con la introducción de la vacuna contra la viruela, al adquirir mayores conocimientos de los procesos causantes de enfermedad y de la capacidad del organismo humano para producir mecanismos de defensa en contra de diversas enfermedades infectocontagiosas, se definieron las estrategias de salud pública que modificaron sustancialmente las políticas en esta materia y que se han seguido modificando de acuerdo con la situación epidemiológica y con la disponibilidad de recursos.
Históricamente las modificaciones en los esquemas de vacunación y las diferentes estrategias seguidas, han posicionado a nuestro país como uno de los ejemplos a seguir en Latinoamérica y entre muchos otros países de medianos ingresos en el campo de la vacunación infantil.
A partir de la introducción de la vacuna contra la viruela el número de inmunógenos (vacunas) en el esquema de vacunación en México se ha ido incrementando en forma progresiva (Cuadro 22).
| Cuadro 22. Incremento de inmunógenos | |
| Año | Vacuna |
| 1926 | Viruela |
| 1948 | DP |
| 1951 | BCG |
| 1954 | DPT/T |
| 1956 | Polio Salk |
| 1961 | Polio Sabin |
| 1970 | Antisarampión |
En 1973 se creó el Programa Nacional de Inmunizaciones en México con importantes modificaciones realizadas de manera progresiva y hasta la fecha (Cuadro 23).
| Cuadro 23. Programa Nacional de Inmunizaciones | |
| 1973 | Programa Nacional de Inmunizaciones: BCG (1), Sabin (3), DPT (3), antisarampión (1) y toxoide tetánico (2) |
| 1974 | Campaña Nacional de Vacunación con 4 vacunas esenciales y un total de seis antígenos, más toxoide tetánico |
| 1974 | Programa Ampliado de Inmunizaciones de la OMS (similar al empleado en México) |
| 1978 | Decreto para la obligatoriedad del uso de la Cartilla Nacional de Vacunación |
| 1980 | Se iniciaron las “Semanas Nacionales de Vacunación” contra poliomielitis y sarampión |
| 1986 | Se agregaron los “Días Nacionales de Vacunación” antipoliomielítica |
| 1998 | BCG; VOP; DPT; sarampión, *rubéola y parotiditis: triple viral (SRP) |
| 1999 | BCG; VOPO; SRP; difteria, tosferina, tétanos, *hepatitis B y *Haemophilus influenzae tipo b (pentavalente) |
| 2004 | BCG; VOP; SRP; pentavalente, *antiinfluenza |
| 2006 | BCG; VOP; SRP, pentavalente, antiinfluenza, *neumococo conjugada heptavalente y *antirrotavirus |
| 2007 | BCG; SRP; *pentavalente con difteria, tétanos y pertussis acelular (DPaT), Hib y *antipoliomielitis parenteral (VIP), *hepatitis B al nacimiento, antiinfluenza; neumococo conjugada heptavalente y antirrotavirus universal |
| 2010 | BCG; SRP; pentavalente con DPaT, Hib y VIP, hepatitis B al nacimiento, antiinfluenza; neumococo conjugada heptavalente y antirrotavirus Universal *Vacuna contra virus del papiloma humano (niñas en CdMx y en municipios con menor desarrollo) |
| 2011 | BCG; SRP; pentavalente con DPaT, Hib y VIP, hepatitis B al nacimiento, antiinfluenza; neumococo conjugada heptavalente antirrotavirus universal, *vacunación universal contra el virus del papiloma humano para las niñas de sexto año de primaria |
Actualmente el Programa Nacional de Vacunación está diseñado para su aplicación “universal” en toda la población pediátrica (Cuadro 24).
| Cuadro 24. Esquema de vacunación en México | ||||||
| MEX | 1 | 2 | 3 | 4 | 5 | 6 |
| BCG | RN | |||||
| HepB ped. | RN | M2 | M6 | |||
| DTPHib | ||||||
| DTPHibHepB | ||||||
| DTPHibHepBIPV | M2 | M4 | M6 | M18 | ||
| DTPHibIPV | M2 | M4 | M6 | M18 | ||
| DTP | A4 | |||||
| IPV | ||||||
| OPV | ||||||
| Neumo Conj. | M2 | M4 | M12 | |||
| Rotavirus | M2 | M4 | M6 | |||
| SRP | A1 | A5 | ||||
| Td | 15 A | |||||
| Tdap | Después de la semana 20 de gestación | |||||
| VPH | A10 | A11 | ||||
| Fuente:Informe País. OPS/OMS. | ||||||
En 1990 se realizó la Cumbre Mundial a favor de la Infancia (ONU) donde México se trazó las siguientes metas: alcanzar coberturas de vacunación mayores de 90% en menores de 1 año. Eliminar el tétanos neonatal. Erradicar la poliomielitis en el año 2000. Reducir en 95% la mortalidad y la morbilidad por sarampión en el año 1995.
Dosis y vía de administración: 0.1 cc intradérmica.
Esquema: dosis única al nacimiento.
Efectos adversos: dolor leve en el sitio de la aplicación y leve reacción “supurativa” que se presenta entre las cuatro y 12 semanas después de la aplicación, con cicatriz posterior.
En casos aislados puede haber reacción con crecimiento ganglionar en la región axilar y/o cervical del mismo lado de la aplicación. En aproximadamente 2% puede haber reacciones locales (absceso en el sitio de la vacuna, adenitis regional).
La vacuna BCG se introdujo en el programa de vacunación en México en 1951, protege parcialmente contra el desarrollo de enfermedad tuberculosa pero principalmente protege de manera eficiente contra las formas graves de tuberculosis como la meningitis tuberculosa o la tuberculosis miliar.
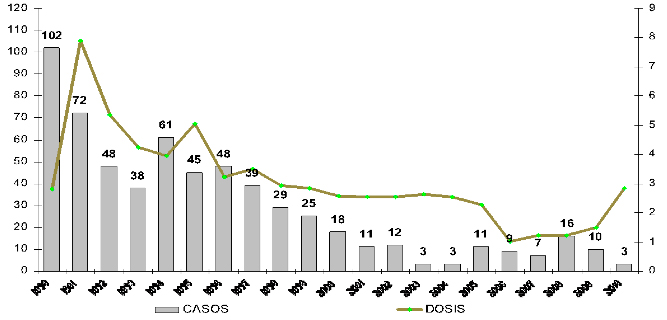
En la Figura 13 se observa la disminución de casos de tuberculosis meníngea y su relación con el número de vacunas aplicadas en México.
Figura 13

Distribución histórica de casos de tuberculosis meníngea en niños menores de 5 años y millones de dosis de BCG aplicadas. México, 1990–2010. Fuente: DGE/CENSIA/Secretaría de Salud.
Dosis y vía de administración: 0.5 cc, inyección intramuscular (vacuna pentavalente: IPV + DTOa + Hib).
Esquema: vacunación primaria, tres dosis en los primeros seis meses de vida, primera dosis a las seis a ocho semanas de edad y posteriormente dos dosis con intervalos entre seis y ocho semanas entre sí y un refuerzo a los 18 meses de edad.
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontàneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación que desaparecen de manera espontánea.
El inicio de la vacunación antipoliomielítica en México se realizó en 1956 utilizando vacuna Salk por vía intramuscular, en 1961 se introdujo la vacuna Sabin de virus vivos atenuados administrada por vía oral y se modificó el esquema mediante suspensión de la vacuna parenteral, aprovechando la facilidad para la administración de la vacuna Sabin, así como su potencial acción a nivel intestinal, sitio habitual de entrada del virus de polio “salvaje”.
Al dejar de circular en nuestro país el virus “salvaje”, se identificaron varios casos de enfermedad paralítica ocasionados por virus vacunal, lo que motivó el dejar de utilizar la vacuna oral (OPV) de virus vivos atenuados (Sabin) para las tres dosis iniciales a los dos, cuatro y seis meses de edad, sustituyéndola por vacuna parenteral de virus muertos (IPV); con esta medida se evita el riesgo de presentar enfermedad por el virus vacunal de la polio.
En la actualidad se utilizan las primeras dosis con vacuna parenteral incluida en la vacuna pentavalente y en dosis de refuerzo se puede utilizar la vacuna Sabin (oral).
En la Figura 14 se observa la disminución de casos de poliomielitis y su relación con el número de vacunas aplicadas.
Figura 14
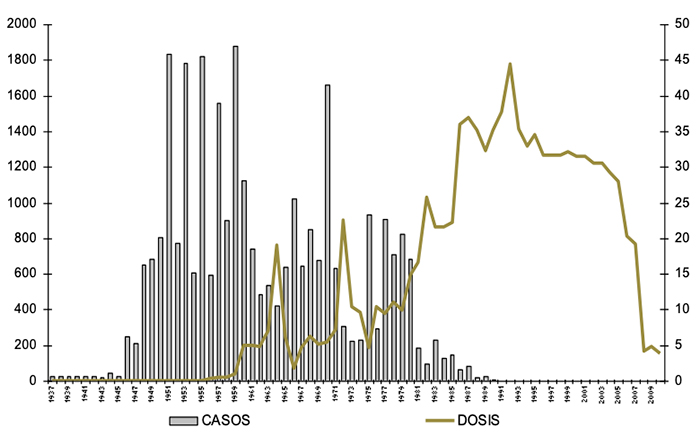
Distribución histórica de casos de poliomielitis y millones de dosis de vacuna antipoliomielitis aplicadas. México, 1937–2010. Fuente: DGE/CENSIA/Secretaría de Salud.
El último caso de poliomielitis ocasionada por el “virus salvaje” en la República Mexicana se registró en Tomatlán, Jalisco, en octubre de 1990 y en 1994 se certifica la eliminación del poliovirus salvaje en las Américas.
En el año 2004, en el estado de Tabasco, se presentó un caso de poliomielitis posvacunal en un menor de un año y en 2006 se registró otro caso en el estado de Hidalgo. Se sabe que la vacuna OPV por ser una vacuna de virus vivos “atenuados” puede producir la enfermedad en forma esporádica (1 caso en 4 a 7 millones de dosis aplicadas), mientras que la vacuna IPV por ser una vacuna hecha a base de virus muertos, no tiene esa posibilidad.
En México, con la introducción de la vacuna antipoliomielítica parenteral (IPV) a través de la vacuna pentavalente en el año 2007, se evita el riesgo de que se vuelvan a presentar casos de poliomielitis posvacunal.
Desde el año 2018 la OMS recomendó que la vacuna de polio oral solamente tuviera las fracciones de polio 1 y polio 3, eliminando la polio 2 en la vacuna con el propósito de suprimir el riesgo de presentación de enfermedad debida al virus vacunal.
En los útimos años se ha observado una disminución importante en la cobertura de vacunación antipolio en México (Figura 15).
Figura 15
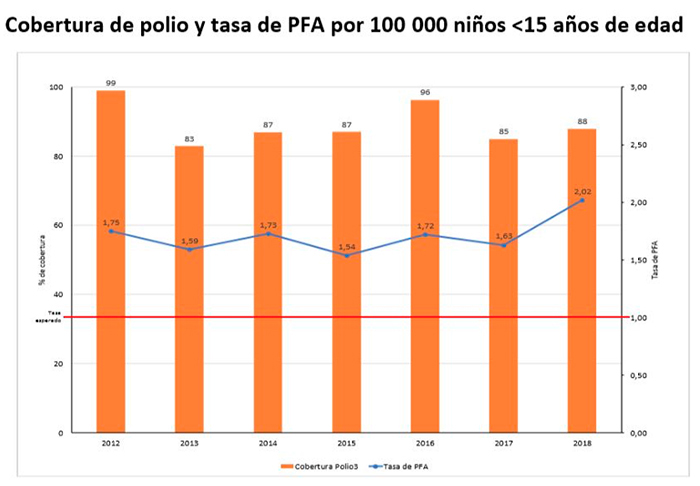
Coberturas de vacunación contra poliomielitis y tasa de “parálisis flácida aguda” en México, 2012-2018. Fuente: Informe País. OPS/OMS.
En la actualidad la vacuna oral “bivalente” (OPV) sólo se utiliza para campañas y después de haber recibido las tres primeras dosis de IPV.
Vacuna contra difteria, tosferina y tétanos (DPT, pentavalente, hexavalente) y difteria-tétanos (Dt).
Dosis y vía de administración: 0.5 cc, inyección intramuscular (vacuna pentavalente: IPV + DTOa + Hib).
Esquema: vacunación primaria tres dosis en los primeros seis meses de vida, primera dosis a las seis a ocho semanas de edad y posteriormente dos dosis con intervalos entre seis y ocho semanas entre sí y un refuerzo a los 18 meses, un refuerzo (DPT) a los cuatro años de edad.
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontàneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación que desaparecen de manera espontánea.
Se recomienda aplicar un refuerzo en la adolescencia a través de cualquiera de las siguientes dos opciones: (dt) vacuna contra la difteria y toxoide tetánico, o DPTa (vacuna contra la difteria, toxoide tetánico y pertussis acelular).
La difteria es una enfermedad causada por un agente bacteriano (Corynebacterium diphteriae), que ataca principalmente las vías respiratorias del huésped y que puede presentar complicaciones graves (dificultad respiratoria, miocarditis, endocarditis).
Desde hace varios años no se han reportado casos del padecimiento en México, debido esencialmente a los programas de vacunación. En la Figura 16 se observa la disminución de casos de difteria y su relación con el número de vacunas aplicadas.
Figura 16
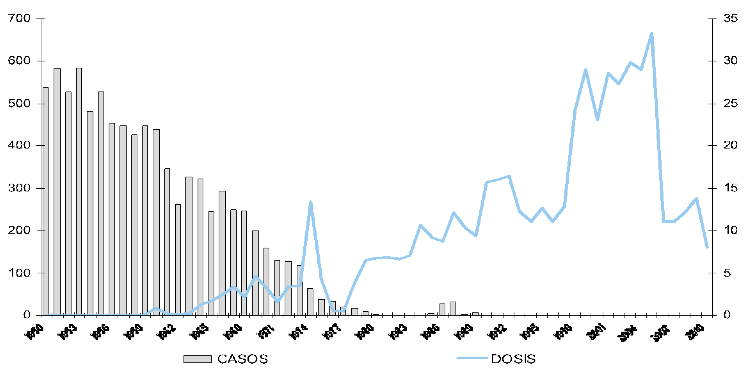
Distribución histórica de casos de difteria y millones de dosis de “vacuna contra la difteria” (DPT, Dt, pentavalente aplicadas). México, 1950–2010. Fuente: DGE/CENSIA/Secretaría de Salud.
En la actualidad se puede considerar que la difteria se encuentra eliminada en México, el último caso registrado se presentó en Lázaro Cárdenas, Michoacán, en octubre de 1990. A pesar de ello, no hay evidencia de que el agente causal esté erradicado, por lo que se mantiene la vacunación dado el riesgo de nuevas epidemias (Figura 16).
Dosis y vía de administración: 0.5 cc, inyección intramuscular (vacuna pentavalente: IPV + DTOa + Hib).
Esquema: vacunación primaria tres dosis en los primeros seis meses de vida, primera dosis a las seis a ocho semanas de edad y posteriormente dos dosis con intervalos entre seis y ocho semanas entre sí y un refuerzo a los 18 meses, y luego un refuerzo (DPT) a los cuatro años de edad.
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontáneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación que desaparecen de manera espontánea.
Actualmente también se recomienda la aplicación de un refuerzo en la adolescencia y en mujeres embarazadas mediante DPTa (vacuna contra la difteria, toxoide tetánico y pertussis acelular ).
La tosferina es una infección respiratoria aguda causada por la bacteria Bordetella pertussis, es una enfermedad con distribución mundial, puede tener complicaciones asociadas como neumonía, sin embargo, por sí misma la infección aguda puede ser grave incluso con mortalidad significativa, particularmente en los recién nacidos y lactantes menores de seis meses de edad. La mejor forma de prevenirla es la vacunación (esquema primario a los dos, cuatro y seis meses de edad, con refuerzos a los 18 meses y a los cuatro años).
Se ha demostrado que también existen formas menos graves que la tos ferina y que se presentan principalmente en adolescentes y adultos, manifestándose como tos crónica de leve o moderada intensidad de varias semanas de duración, con o sin fiebre. Para prevenir estos cuadros y tratar de evitar la persistencia en la cadena de transmisión se ha propuesto la vacunación con una dosis adicional en los adolescentes y adultos.
Un esfuerzo adicional para proteger a los recién nacidos dada su alta mortalidad, es el proyecto denominado “capullo”, que consiste en la vacunación de los padres y de otros adultos que convivan en su domicilio con los recién nacidos. Otra propuesta es la de vacunar a las mujeres embarazadas, procedimiento que se realiza sin riesgo mediante la vacuna acelular que casi no tiene efectos secundarios de importancia.
En la Figura 17 se observa la disminución de los casos reportados de tosferina y su relación con el número de millones de vacunas aplicadas. La Figura 18 muestran las cifras de cobertura de vacunación con inmunógenos contra difteria, tos ferina y tétanos y el registro de casos de difteria y tosferina en México 2012–2018.
Figura 17
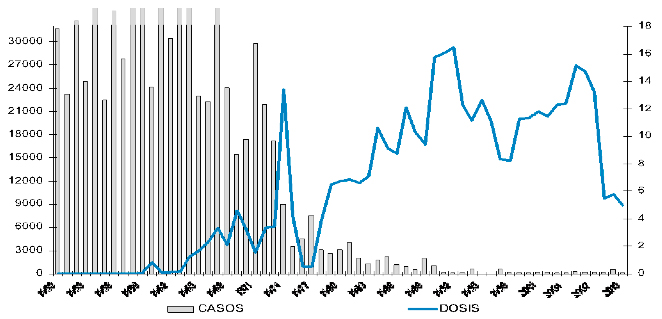
Distribución histórica de casos de tos ferina y millones de dosis de vacuna antipertussis aplicadas. México, 1950–2010. Fuente: DGE/CENSIA/Secretaría de Salud.
Figura 18
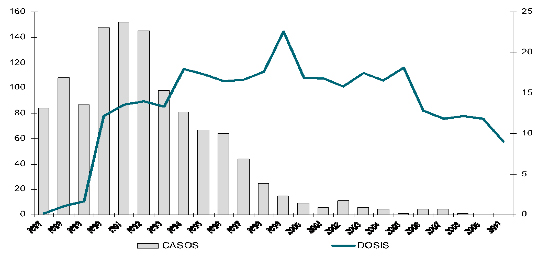
Distribución histórica de casos de tétanos neonatal y millones de dosis de vacuna de tétanos (DPT, tetravalente, pentavalente y Td) aplicadas. México, 1987–2010. Fuente: DGE/CENSIA/Secretaría de Salud.
Dosis y vía de administración: 0.5 cc, inyección intramuscular (vacuna pentavalente: IPV + DTOa + HIb).
Esquema: vacunación primaria tres dosis en los primeros seis meses de vida, primera dosis a las seis a ocho semanas de edad y posteriormente dos dosis con intervalos de seis a ocho semanas entre sí y un refuerzo a los 18 meses de edad, un refuerzo (DPT) a los cuatro años de edad.
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontáneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación que desaparecen de manera espontánea. Posteriormente se recomienda aplicar dosis de refuerzo con 0.5 cc de toxoide tetánico.
El tétanos no es propiamente una infección, sino la consecuencia de la toxina producida por el Clostridium tetani.
Además de controlar los cuadros de tétanos en la población en general, una de las metas propuestas con mayor impacto es el de evitar el tétanos neonatal cuya morbilidad secundaria y mortalidad son elevadas.
En la Figura 18 se observa la disminución de casos de tétanos neonatal y su relación con el número de vacunas aplicadas.
En la Figura 19 se muestran los casos registrados y las defunciones por tétanos neonatal, donde es posible observar que actualmente la meta se ha alcanzado, sin embargo, es necesario continuar con los programas de vacunación para garantizar que la enfermedad no vuelva a presentarse.
Figura 19
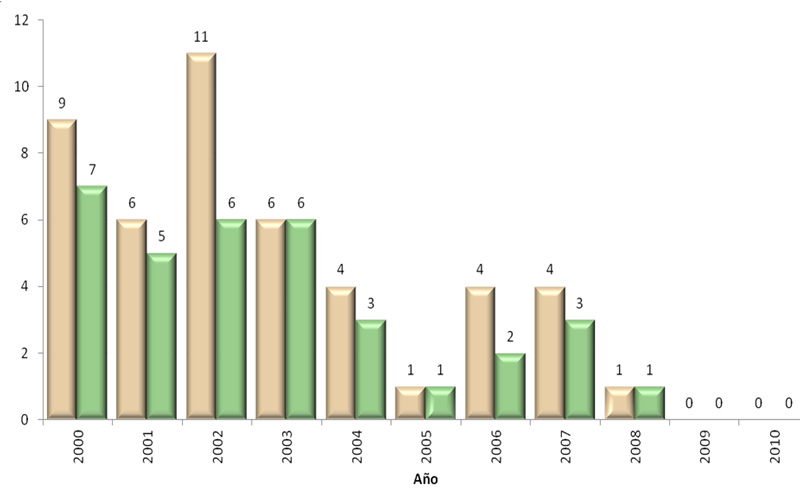
Casos y defunciones por tétanos neonatal. México, 2000–2010. Fuente: DGE/CENSIA/Secretaría de Salud.
En la Figura 20 se muestra el número de casos registrados de tétanos neonatal y de tétanos en otras edades en México 2012–2018.
Figura 20
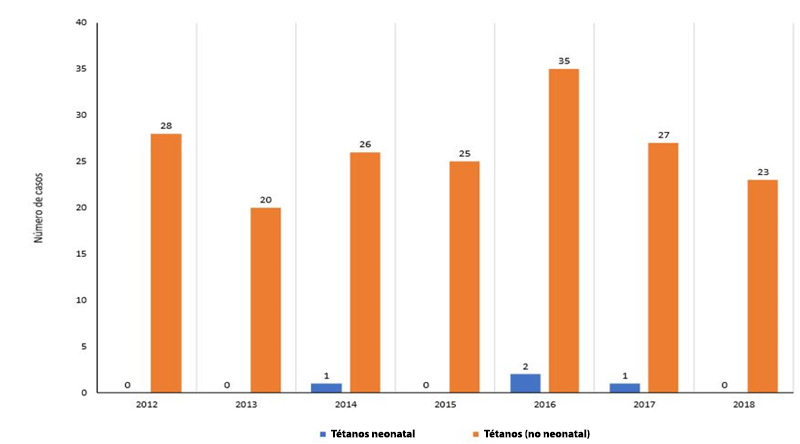
Registro de casos de tétanos neonatal y de tétanos en otras edades en México, 2012–2018. Fuente: Informe País. OPS/OMS
Dosis y vía de administración: 0.5 cc, inyección intramuscular (vacuna pentavalente: IPV + DTPa + Hib).
Esquema: cuatro dosis, primera dosis a las seis a ocho semanas de edad y posteriormente dos dosis con intervalos de seis a ocho semanas entre sí y un refuerzo a los 18 meses de edad.
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontáneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación que desaparecen de manera espontánea.
Las enfermedades “invasivas” y entre ellas la meningitis causada por Haemophilus influenzae tipo B, hasta la década de los 90 ocupaban una importante causa de morbimortalidad en México, principalmente en los menores de cinco años de edad. Con la introducción de esta vacuna en el Programa Nacional de Vacunación a partir de 1997, se logró disminuir la morbimortalidad en forma significativa, de tal manera que actualmente la meningitis causada por H. influenzae tipo B casi ha desaparecido en nuestro medio y no es un diagnóstico a descartar en ningún niño que tenga su esquema de vacunación completo o que incluya al menos tres dosis de esta vacuna.
En la Figura 21 se observa la evidente disminución de los casos de infecciones invasivas por H. influenzae en relación al número de vacunas aplicadas.
Figura 21
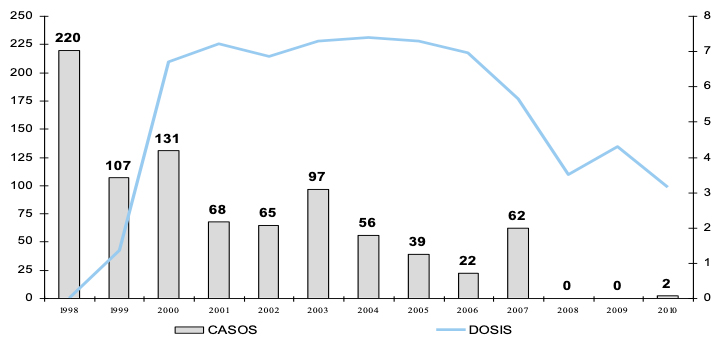
Distribución histórica de casos de infecciones invasivas causadas por Haemophilus influenzae y millones de dosis de vacuna anti-Hib aplicadas. México, 1998-2010. Fuente: DGE/CENSIA/Secretaría de Salud.
Dosis y vía de administración: 0.5 cc, inyección intramuscular.
Esquema: el Programa Nacional de Vacunación en México recomienda la aplicación de tres dosis; iniciando al nacimiento y posteriormente a los dos y seis meses de edad.
En las otras edades cuando el sujeto no haya recibido ninguna dosis se recomienda a cualquier edad la aplicación de tres dosis con dos meses de intervalo entre ellas.
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontáneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación que desaparecen de manera espontánea.
La hepatitis B es una enfermedad viral producida por el virus de la hepatitis B, representa un problema de salud pública a nivel global, la infección crónica causada por este virus puede presentar complicaciones graves como cirrosis hepática y/o cáncer hepatocelular, e incluso puede ocasionar la muerte. La transmisión del virus puede llevarse a cabo en forma perinatal (vertical) y horizontal.
La prevención de la transmisión perinatal del virus de la hepatitis B es particularmente importante en el diseño e implementación de un programa universal de vacunación. Independiente de la vía de adquisición del virus, la forma crónica de la enfermedad se establece generalmente en la infancia temprana y esta posibilidad se debe a la interacción entre el virus y las defensas del huésped.
En los países en donde se ha establecido en forma adecuada un programa universal de vacunación, la infección por el virus de la hepatitis B se encuentra controlada.
Aunque México no está considerado como un país de alta prevalencia de casos de hepatitis B, la inclusión de esta vacuna se acompañó de una disminución importante en el número de casos registrados.
En las áreas de elevada endemicidad, la mayoría de las formas crónicas de la enfermedad se establecen durante la infancia y la niñez temprana. La transmisión madre–hijo es una ruta importante para la permanencia de la endemicidad y a menudo se asocia a complicaciones serias durante la adolescencia o la etapa adulta del enfermo.
El control final y la eliminación del virus de la hepatitis B depende del establecimiento a nivel global de un programa universal efectivo de vacunación y del uso de algunos medicamentos en los casos demostrados de infección.
Vacuna triple viral (parotiditis, sarampión y rubéola).
Dosis y vía de administración: 0.5 cc, inyección subcutánea.
Esquema: al año de edad y refuerzo a los seis años.
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontáneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación que desaparecen de manera espontánea.
En México, gracias a la vacunación contra el sarampión, se ha logrado casi el control de la enfermedad. Cuando se introdujo esta vacuna en el Programa Nacional de Vacunación en 1970, se aplicaba una sola dosis a los nueve meses de edad, después se recomendó su aplicación al cumplir el año de edad. En los años 1989 y 1990 se presentó en el país un brote de sarampión con 68 782 casos y 5 899 defunciones registradas. A partir de entonces, la vacuna se aplica en dos dosis recomendándose al año de edad en forma conjunta con la vacuna de rubéola y parotiditis (MMR) [triple viral] y después un refuerzo en la primaria (aproximadamente a los seis a siete años de edad).
En el año 2006 se presentaron seis casos de sarampión en la Ciudad de México y 17 en el Estado de México, en todos se identificó una cepa “importada” del virus, ya que hasta ese momento no se reportó circulación del virus en México. En los siguientes años se reportaron casos aislados de sarampión, todos considerados “importados”, sin que se registraran muertes por esa enfermedad.
En el año 2020, hasta el 15 de junio, se habían registrado 177 casos en México (dos de ellos en Campeche) y el resto en el área metropolitana de la Ciudad de México; la mayoría en personas no vacunadas o con vacunación incompleta. La aparición de nuevos casos de sarampión ha coincidido con una disminución significativa en las coberturas de vacunación en el país.
En la Figura 22 se muestra la disminución del número de casos de sarampión y su relación con el número de vacunas aplicadas.
Figura 22
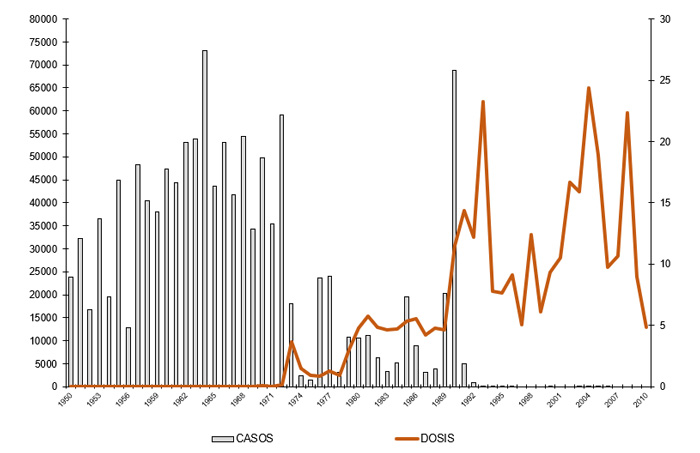
Distribución histórica de casos de sarampión y millones de dosis de vacuna antisarampión aplicadas. México, 1950–2010. Fuente: DGE/CENSIA/Secretaría de Salud.
Las defunciones por sarampión han mostrado un franco descenso como consecuencia de las estrategias de vacunación, en 1990 se reportaron 8 150 defunciones, mientras que en 1995 se reportaron dos defunciones.
Vacuna triple viral (parotiditis, sarampión y rubéola).
Dosis y vía de administración: 0.5 cc, inyección subcutánea.
Esquema: al año de edad y refuerzo a los seis años.
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontáneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación, que desaparecen de manera espontánea.
El objetivo principal de introducir la vacuna anti-rubéola en el Programa Nacional de Vacunación fue el de alcanzar altas coberturas y prevenir la presentación de casos de rubéola congénita. En la Figura 23 se observa la tasa de incidencia y el número de casos de rubéola registrados de 1990 a 2010.
En el periodo 1990-1997 correspondiente a la época prevacunal, se notificaron a la Dirección General de Epidemiología 391 288 casos de rubéola. De 1998 hasta el año 2000 se notificaron 84 770 casos, lo que representa una disminución del 78.3%. En el año 2008 se reportaron sólo 46 casos con una disminución del 99.9%, esto permitió interrumpir la transmisión endémica de la rubéola. En los últimos años no se han registrado casos de rubeóla congénita en México, coincidiendo esta disminución con la baja ostensible en la morbilidad por esta enfermedad y con la cobertura masiva de vacunación (Figuras 23 y 24).
Figura 23
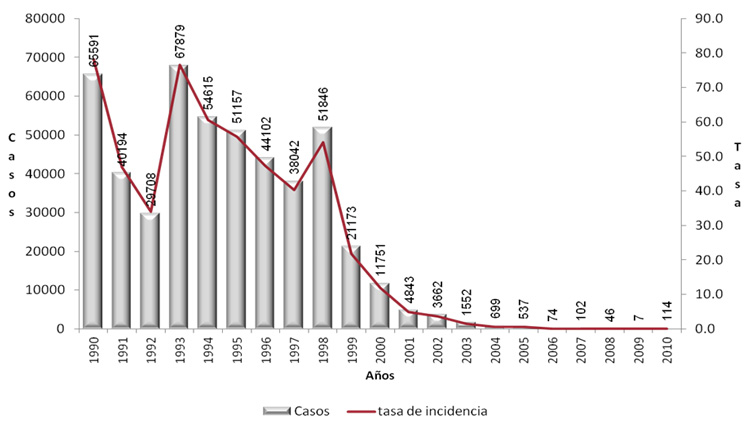
Casos e incidencia de rubéola en México, 1990- 2010. Fuente: DGE/CENSIA/Secretaría de Salud.
Vacuna triple viral (parotiditis, sarampión y rubéola).
Dosis y vía de administración: 0.5 cc, inyección subcutánea.
Esquema: al año de edad y refuerzo a los seis años.
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontáneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación, que desaparecen de manera espontánea.
La parotiditis es una infección producida por el virus de la parotiditis, considerada generalmente como “benigna” pero que puede tener repercusiones importantes a nivel genital e incluso puede producir esterilidad; su morbilidad ha disminuido considerablemente a partir de la introducción de la vacunación de manera rutinaria a través de la vacuna triple viral (conjuntamente con sarampión y rubéola) y el esquema actualmente utilizado es la dosis primaria al año de edad y aplicación de un refuerzo a la entrada a la primaria (seis a siete años de edad).
Posteriormente se recomienda la aplicación de una dosis adicional de vacuna combinada de sarampión y rubéola durante la adolescencia.
Vía de administración: oral.
Esquema: vacuna monovalente (Rotarix®), dos dosis, iniciando a las seis a ocho semanas de edad y segunda dosis aproximadamente seis a ocho semanas después; es importante concluir el esquema a los seis meses de edad o antes.
Vacuna pentavalente Rotatec®
Tres dosis, iniciando a las seis a ocho semanas de edad y dosis posteriores con intervalos de aproximadamente seis a ocho semanas, es importante concluir el esquema a los seis meses de edad o antes.
La gastroenteritis por infección con el rotavirus en los lactantes se ha considerado una de las principales causas de morbimortalidad por diarrea en ese grupo de edad, por eso el desarrollo de una vacuna eficaz y segura, en cuya fase de investigación clínica participaron grupos de investigadores mexicanos (New England Journal of Medicine, 05 Ene 2006). Se incluyó en el año 2007 en forma universal en el Programa Nacional de Vacunación para su aplicación en esquema completo antes de los seis meses de edad, esto ha permitido disminuir de manera importante la mortalidad por diarrea en los menores de cinco años.
Vacuna monovalente Rotarix®
Dos dosis, iniciando a las seis a ocho semanas de edad y una dosis posterior con intervalos de aproximadamente seis a ocho semanas, es importante concluir el esquema a los seis meses de edad o antes.
Actualmente existe disponibilidad de dos diferentes vacunas igualmente eficaces y seguras. Una monovalente cuyo esquema incluye la aplicación de dos dosis, la primera a los dos meses de edad y la segunda a los cuatro meses; y una pentavalente cuyo esquema requiere de tres dosis para ser aplicadas a los dos, cuatro y seis meses de edad.
En la Figura 25 se ilustra la disminución de la morbilidad y la mortalidad por diarrea en < 1 año, entre 1 y 2 años y en < 5 años de edad, a partir de la inclusión de esta vacuna en el Programa Nacional de Vacunación.
Figura 25
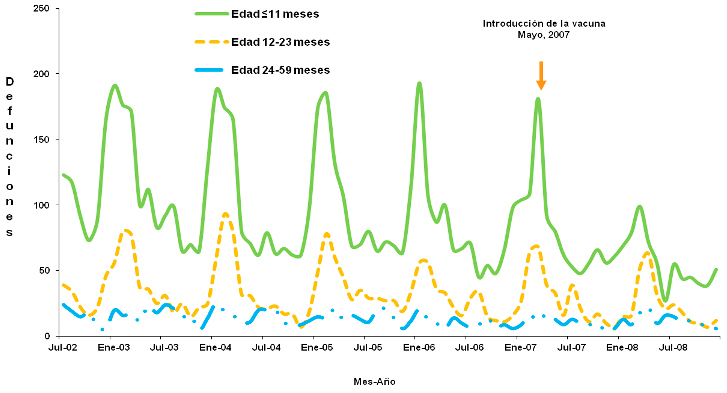
Defunciones por diarrea en niños menores de 11 meses, 12 a 23 y 24 a 54 meses de edad. México, 2003-2009. Fuente: DGE/CENSIA/Secretaría de Salud.
Dosis y vía de administración: 0.5 cc, inyección intramuscular.
Esquema: dos a tres dosis en los primeros seis meses de vida y un refuerzo al año de edad.
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontáneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación, que desaparecen de manera espontánea.
La neumonía por neumococo en nuestro país se ha identificado como causa importante de morbilidad y mortalidad, principalmente en el grupo etario de menores de cinco años. Desde su inclusión en el Programa Nacional de Vacunación en el año 2006 con una vacuna conjugada heptavalente (siete diferentes cepas del neumococo), hasta la actualidad en que se cuenta con dos vacunas eficaces y seguras contra estas enfermedades, una de trecevalente (13 cepas diferentes) y otra decavalente (10 cepas diferentes), ha permitido disminuir la morbimortalidad en este grupo de edad (Figuras 26 y 27).
Figura 26
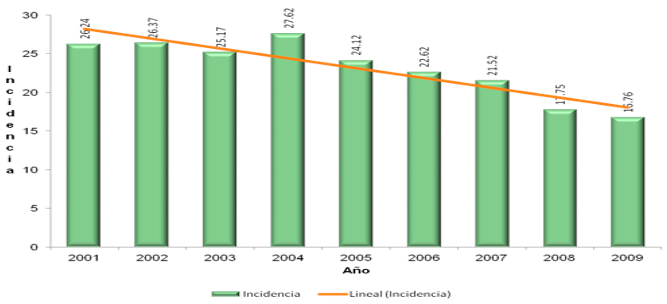
Incidencia y casos de neumonía en menores de cinco años. México 2000-2009. Fuente: DGE/CENSIA/Secretaría de Salud.
Figura 27
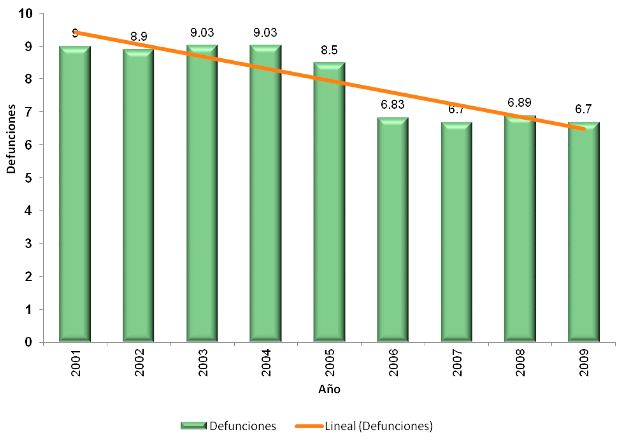
Tasa de mortalidad por neumonía en < 5 años. México, 2000-2009. Fuente: DGE/CENSIA/Secretaría de Salud.
Dosis y vía de administración: 0.5 cc, inyección intramuscular.
Dosis: una dosis primaria y un refuerzo uno o dos meses después de la primera dosis, posteriormente una dosis cada año al inicio del periodo invernal.
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontáneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación, que desaparecen de manera espontánea.
La vacuna contra el virus de la influenza ha sido utilizada durante muchos años como la principal herramienta para prevenir esta enfermedad y sus complicaciones. La influenza es una enfermedad que afecta a todas las edades a nivel mundial, que tiene un impacto importante a nivel social y económico, ya que es una de las principales causas de inasistencia laboral y escolar. Aunque la mayoría de los casos pueden considerarse de evolución benigna, puede ser causa de mortalidad principalmente en las edades ubicadas en los extremos de la vida (< 2 años y adultos mayores); en casos de epidemias causadas por virus de la influenza de mayor patogenicidad, la mortalidad asociada puede llegar a cifras mayores del 50% (influenza española, pandemia de 1918, Influenza aviar en los primeros años del siglo XXI localizada en algunos países asiáticos).
Algunos países de altos ingresos como Estados Unidos han ampliado su esquema y recomiendan la vacunación universal (todas las edades), mientras que otros como México mantienen la vacunación universal para < 5 años y > 60 años, además de insistir en la vacunación a cualquier edad en poblaciones consideradas de mayor riesgo (embarazadas, casos de enfermos con diabetes, neumopatía crónica, hipertensión arterial, obesidad mórbida, etc.). Sin embargo, la vacunación se recomienda a toda la población mayor de seis meses de edad en forma anual.
Actualmente las vacunas contra la influenza contienen tres o cuatro diferentes tipos de antígeno; virus de Influenza “A” H1N1, Influenza “A” H3N2 e Influenza “B” Victoria y Yamagata.
Aunque la Influenza se ha considerado una enfermedad benigna, es una de las principales causas de ausentismo laboral y escolar con la consecuente afectación económica en las familias y en la sociedad, también sigue teniendo mortalidad asociada como se observa en la Figura 28.
Dosis y vía de administración: 0.5 cc, inyección intramuscular (tres dosis).
Recomendación a nivel internacional (tres dosis): día cero, dos y seis meses después de la primera dosis.
Programa nacional México (dos dosis): niñas de 5º de primaria u 11 años de edad: día 0 (primera dosis), y seis meses después (segunda dosis).
Eventos adversos: puede haber dolor, rubor e inflamación leve en el sitio de la aplicación que cede espontàneamente en las primeras 24 h. En porcentajes menores al 10% de los casos puede haber fiebre, falta de apetito y somnolencia durante las 48 h siguientes a su aplicación que desaparecen de manera espontánea.
Actualmente se conoce que el virus del papiloma humano es el causante del 80 al 85% del cáncer cervicouterino en México. La infección se adquiere por contacto sexual y suele cursar completamente asintomático durante 20 años o más, por lo que pasa totalmente inadvertida para después presentarse la enfermedad, que puede ser diagnosticada tempranamente a través de estudios de “Papanicolau” o presentarse en etapas más avanzadas con síntomas y signos evidentes, en cuyo caso tiene una elevada morbilidad y mortalidad asociada.
Se ha demostrado que las vacunas autorizadas para prevenir esta enfermedad son eficaces y seguras. Para obtener mayor eficacia es conveniente aplicar el esquema antes de iniciar las relaciones sexuales, en la mayoría de los países se recomienda su aplicación a partir de los 10 años de edad. La aplicación en las niñas del esquema completo previene la enfermedad, mientras que en los varones previene la posible diseminación de la infección.
Internacionalmente se recomienda la aplicación de tres dosis con intervalos de dos y seis meses a partir de la primera dosis (1ª dosis = día cero; 2ª dosis = dos meses después de la primera, y 3ª dosis = seis meses después de la primera).
En México el Programa Nacional de Vacunación que el sector salud proporciona a las niñas de 11 años de edad de manera universal y gratuita, incluye un esquema diferente, con dos dosis (1ª dosis = día 0, y 2ª dosis = seis meses después de la primera dosis).
Si la persona inicia su vacunación contra el virus del papiloma después de los 14 años de edad, se recomienda utilizar el esquema de tres dosis. En los dos esquemas su eficacia ha sido comprobada.
Existen dos vacunas autorizadas: Gardasil® y Cervarix®, ambas han demostrado ser seguras y eficaces para la prevención del cáncer cervicouterino ocasionado por este virus.
Vale la pena hacer notar la disminución en la cobertura de vacunación general en México en los últimos años, principalmente en la vacunación contra: poliomilelitis, difteria, tosferina, tétanos, Haemophylus influenzae, hepatitis B (pentavalente), rotavirus y neumococo, como se observa en la Figura 29.
En el Programa Nacional de Vacunación existen dos inmunógenos (vacunas) con la recomendación de ser aplicadas al nacimiento (primeras 24 h), la vacuna contra la tuberculosis (BCG) y la vacuna contra la hepatitis B. El propósito de esta indicación es proteger a todos los recién nacidos contra estas enfermedades con el conocimiento que aún a esta edad se obtiene una respuesta inmunológica adecuada.
La vacuna contra la tuberculosis protegerá al menor de las formas graves de la enfermedad (meningitis, tuberculosis miliar, etc.).
La aplicación contra la hepatitis B en el recién nacido tiene como propósito iniciar en forma temprana la protección contra esa infección, especialmente del riesgo de la transmisión de la enfermedad por parte de la madre; de cualquier forma, se deberá completar el esquema completo de tres dosis de la vacuna con aplicaciones subsiguientes en intervalos de cerca de ocho semanas para asegurar razonablemente la protección definitiva. Su aplicación al nacimiento es fundamental si se pretende lograr la erradicación de la enfermedad.
La vacunación debe realizarse en todo recién nacido sano que se encuentre en condiciones de estabilidad clínica, esto incluye a recién nacidos prematuros en quienes se ha demostrado una adecuada respuesta inmunológica. La excepción son los recién nacidos que pesen < 2 kg, en cuyo caso la vacunación puede ser diferida hasta que el menor alcance los 2 kg de peso.
En los casos de enfermedad aguda o inestabilidad clínica deberá diferirse el inicio o la continuación del esquema de vacunación hasta completarlo.
Durante mucho tiempo en México se pensó que la vacunación solamente resultaba útil cuando se aplicaba en los niños pequeños o en casos de prevención específica (rabia, tétanos, etc.), sin embargo, en la actualidad existen razones y recomendaciones para el uso de vacunas en las diferentes edades.
Específicamente en la adolescencia se recomienda el uso de vacunas con fines de: prevención rutinaria y prevención de riesgos específicos.
La adecuada información y aceptación de la vacunación por el personal de salud es un factor determinante para la vacunación en cualquier país.
Una estrategia utilizada en países de altos ingresos es el requerimiento de la vacunación completa en las escuelas secundarias, intervención que podría ser utilizada en aquellos países con elevada cobertura escolar.
Se esperan en un futuro próximo nuevas vacunas para el adolescente y esto representará un reto más en la plataforma de vacunación para este grupo de edad. Las elevadas coberturas de vacunación en niños se han establecido a través de los años, por lo que el éxito en la implementación del esquema de vacunación en el adolescente requiere de tiempo, recursos, voluntad política, etcétera.
La disminución o falta de la inmunidad por bajas coberturas en el adolescente representa un riesgo para el desarrollo de enfermedad a edades mayores, asimismo, este acúmulo de susceptibles puede favorecer la aparición de brotes epidémicos de enfermedades como sarampión o hepatitis A. La mayoría de los adolescentes han recibido al menos una dosis de vacuna contra difteria, tétanos y tos ferina (DPT) en la niñez, hay evidencia de que la inmunidad contra tétanos y difteria disminuye a los 10 años y para pertussis a los cinco y 10 años, por lo tanto hay una gran cantidad de adolescentes y adultos susceptibles de presentar la enfermedad o en el caso de pertussis, además ser un reservorio importante y fuente de infección para sujetos susceptibles.
La vacunación en el adolescente puede reducir el riesgo de infección en edades mayores, disminuir la transmisión de la infección a grupos de riesgo, y ayudar a reforzar la importancia de la vacunación en los padres y el personal de salud.
En México esta enfermedad se ha eliminado, registrándose el último caso en Lázaro Cárdenas, Michoacán, en octubre de 1991. A pesar de ello no hay evidencia de que el agente causal esté erradicado, por lo que se mantiene la vacunación dado el riesgo de nuevas epidemias, como ha sucedido en países como Rusia, que habían logrado el control de la enfermedad y en los años 90 ocurrió un aumento del número y gravedad de los casos en los adultos, relacionado con una pérdida de la inmunidad. La encuesta seroepidemiológica realizada en 1995 demostró que 50% de los mayores de 18 años estudiados eran susceptibles a difteria, lo que indujo a cambiar la vacuna TT por Td en 1997.
Pertussis (tosferina) representa una de las enfermedades que siendo prevenible por vacunación ha mostrado en algunos países un aumento dramático en los últimos 30 años. En Estados Unidos (EU) a principios de los años 80 se notificaban menos de 2 500 casos anuales, en contraste con más de 15 000 casos notificados en el año 2006.
Debido a que la inmunidad contra pertussis inducida por vacuna disminuye después de cinco a 10 años, los adolescentes constituyen el grupo de mayor riesgo para contraer la enfermedad y son considerados como el principal reservorio para su transmisión.
Pertussis es aún causa de brotes principalmente en niños pero también en adolescentes y adultos.
La tosferina en el lactante es más grave e inclusive puede ser fatal. Noventa porciento de los fallecimientos por esta causa se presenta en menores de un año no vacunados. El espectro clínico de la enfermedad varía desde la presencia clásica del síndrome coqueluchoide (tos quintosa, disneizante, cianozante y silbido inspiratorio) o apneas en el menor de tres meses, lo que puede dificultar su diagnóstico. En adolescentes y adultos jóvenes la infección puede ser asintomática, presentarse como un cuadro catarral inespecífico; sin embargo, hasta en 16% de los adolescentes y 28% de los adultos se pueden presentar complicaciones como neumonía y se reporta que puede ser causa de hospitalización en 1.5 y 3.5% de los casos, respectivamente.
Se ha documentado que pertussis puede ser causa de tos de evolución crónica en el adolescente y en el adulto mayor, particularmente en aquellos con factores de comorbilidad como patología respiratoria crónica, cardiaca, o enfermedad neuromuscular.
En los pacientes asintomáticos, la nasofaringe se coloniza en forma transitoria, los portadores pueden transmitir la infección a individuos susceptibles no vacunados o con esquema incompleto de vacunación, que habitualmente son los menores de seis meses, pero también pueden ser sujetos de cualquier edad que hayan disminuido sus niveles de protección. La información indica, que de los lactantes con tos ferina confirmada en los que se documenta la fuente de infección, 83% corresponde a contacto intradomiciliario, de ellos 55% corresponde a los padres. Debido a la gravedad de la tos ferina en este grupo de edad, se ha establecido la estrategia “Capullo”, que consiste en la vacunación de los contactos con la probabilidad de transmitir la enfermedad al recién nacido, vacunación a la madre en el periodo concepcional o en el posparto inmediato y a los miembros de la familia antes del contacto con el recién nacido. La protección se alcanza aproximadamente una semana después de aplicado el refuerzo.
La vacunación contra pertussis en el adolescente ofrece la posibilidad de disminuir los casos de tos ferina en la comunidad en todos los grupos de edad.
A diferencia de la vacuna DPT que contiene la bacteria completa de la Bordetella pertussis, las vacunas acelulares sólo contienen algunos antígenos de la misma, lo cual las convierte en menos reactogénicas pero inmunogénicamente comparables.
Debido a las reacciones locales y sistémicas atribuibles a las vacunas con células completas, como dolor, eritema, aumento de volumen, irritabilidad, fiebre, hipotonía, etc., estas vacunas están contraindicadas después de los seis años de edad.
En el 2005 fueron licenciadas por la FDA en Estados Unidos dos vacunas de pertussis acelular combinadas con tétanos y difteria (Tdap), también disponibles en México: Boostrix® (GSK), para uso en edades de 10 a 18 años; Adacel®, para personas de 11 a 64 años.
Actualmente en varios países se ha indicado el refuerzo con Tdap en el adolescente, en EU desde el 2006 se recomienda la aplicación de Tdap entre los 11 y 12 años de edad o entre los 13 y 18 años, si no han recibido el refuerzo con Td.
En México se ha observado una tendencia a la disminución de los casos de tétanos. Durante el periodo de 2000 a 2007, se registraron 528 casos en hombres y 116 en mujeres, la mayoría de los cuales se presentaron en adultos. Durante el lapso 2018-2019, 21 y 34 casos, respectivamente.
En México la vacunación de refuerzo con toxoide tetánico después de los siete años de edad está indicada en toda la población. Habitualmente se administra en combinación con toxoide diftérico (d). Debido a la menor cantidad de dosis de toxoide diftérico, la posibilidad de reacciones secundarias en niños mayores y adultos es menor. Se recomiendan dos dosis con un intervalo de uno a dos meses entre sí. Además de la prevención del tétanos en cualquier grupo de edad, una meta importante principalmente en países de medianos ingresos es la prevención del tétanos neonatal. La mujer embarazada debe recibir durante la gestación dos dosis de toxoide tetánico con al menos cuatro semanas de diferencia entre la primera y la segunda dosis, debe aplicarse por lo menos dos semanas antes del parto.
También existe en México un programa para aplicar vacuna Td en embarazadas.
La cobertura nacional de vacunación con dos dosis de Td en mujeres en edad fértil fue de 67.3% según el reporte Ensanut del año 2012.
Los pacientes que presentan cuadro clínico de tétanos deben recibir en el periodo de convalecencia de la enfermedad toxoide tetánico, ya que la enfermedad no confiere inmunidad.
La infección por rubéola tiene una distribución universal, con una mayor incidencia en los meses de invierno y primavera; el periodo de transmisión es unos días previos al inicio de los síntomas y hasta siete días después del exantema. Aproximadamente 25 al 50% de las infecciones son asintomáticas, en la niñez esta enfermedad es generalmente benigna, su mayor impacto se presenta cuando afecta a la mujer embarazada, condicionando aborto, muerte fetal y malformaciones congénitas que incluyen el síndrome de rubéola congénita. Por ello las metas de la OMS de la vacunación contra la rubéola es la eliminación del síndrome de rubéola congénita (SRC), principalmente cuando la infección se adquiere o se está en contacto con enfermos de rubéola durante el primer trimestre del embarazo. Si la infección ocurre en las primeras ocho semanas de gestación, 85 al 90% de los productos presentarán algún defecto congénito.
Las encuestas seroepidemiológicas realizadas en México indican que aproximadamente 20% de las mujeres en edad fértil son susceptibles a rubéola.
En México el registro de casos de SRC se inició a partir de 1998, en 1997 se registró un brote de rubéola en La Paz, Baja California, lo que permitió identificar una prevalencia del SRC de 4.08%. En 1998 en Tamaulipas, en 58 mujeres embarazadas expuestas durante un brote en el que se registraron 2 800 casos de rubéola, la incidencia del SRC fue de 0.144.
Durante 2004 se registraron cinco casos, en 2005 un caso en el estado de Veracruz; durante 2018 y 2019 no se notificaron casos de rubéola congénita en el país. Durante 2008 se notificaron a la Dirección General Adjunta de Epidemiología, cuatro casos de SRC de los estados de Nuevo León, Puebla, Tabasco y Yucatán.
A partir de 2004, México se incorporó al Plan para la Eliminación de la Rubéola y del SRC, vacunando con SR a la población de 13 a 39 años de edad. De marzo a mayo de 2008, se realizó la Campaña Nacional para la Eliminación de la Rubéola y el Síndrome de Rubéola Congénita en la población de 19 a 29 años de edad, lográndose vacunar un 99.7% de la meta programada.
En México casi 1:5 nacimientos ocurre en una mujer embarazada (aproximadamente 400 000 casos anuales de embarazos en adolescentes), por lo tanto es conveniente que todas las adolescentes reciban vacuna contra la rubéola antes de iniciar un embarazo.
El sarampión es una enfermedad infecciosa altamente contagiosa de etiología viral y distribución universal que se presenta predominantemente en la edad pediátrica, aunque puede manifestarse también en adolescentes y adultos; a menudo presenta complicaciones y puede ser mortal. Dentro de las complicaciones se encuentran: encefalitis, neumonía, bronquiolitis, otitis media, diarrea y panencefalitis esclerosante subaguda. En los países con vacunación universal, el número de casos en los últimos años ha disminuido significativamente, lo que ha permitido su control, no obstante hay países en los que el sarampión es una causa importante de morbilidad y mortalidad y pueden ser una fuente de transmisión a individuos susceptibles y presentarse transmisión a países aun con elevadas coberturas de vacunación.
En México, después de tres años de no existir la circulación del virus del sarampión (de 1997 a 1999), en el año 2000 se presentaron 30 casos considerados como programáticamente no prevenibles por vacunación, en la Ciudad de México, Sinaloa, Baja California y Estado de México. En el año 2001 se presentaron tres casos en Quintana Roo, importados de Estados Unidos. Para el año 2002 no se registraron casos. En el 2003 se registraron 44 casos y en el 2004, 64 casos de sarampión en: Ciudad de México (43), Estado de México (15), Hidalgo (3), Coahuila (2) y Campeche (1), reportándose el último de ellos en la semana epidemiológica núm. 17.
Durante el 2005 se registraron seis casos de sarampión, en el 2006 se presentaron seis casos en la Ciudad de México y 17 en el Estado de México. En el año 2019 se reportaron 20 casos de sarampión asociados a importación. En 2020 en la Ciudad de México se habían cuantificado más de 170 casos, la mayoría de ellos en jóvenes y adultos sin adecuado esquema de vacunación, coincidiendo también con una disminución en las coberturas a nivel nacional.
La vigilancia y el mantenimiento de coberturas altas de vacunación primaria y los refuerzos contra el sarampión son esenciales para su eliminación y erradicación.
En México se aplica la vacuna SR a los sujetos de 13 a 39 años.
La infección por el virus de la hepatitis B (HB) es un problema global de salud pública con alrededor de 2 billones de individuos infectados y 350 millones con infección crónica en el mundo. La OMS estimó que en el año 2002 la HB fue causa de 600 000 fallecimientos en el mundo, como resultado fundamentalmente de complicaciones como cirrosis y cáncer hepático.
La OMS ha clasificado a los países con base en el resultado de los estudios seroepidemiológicos de prevalencia del antígeno de superficie en tres niveles: 1. Baja endemicidad (< 2% Europa occidental, EU y Australia); 2. Endemicidad media (2-8% Sudamérica y Europa oriental) y 3. Endemicidad elevada (≥ 8% África, Asia excepto Japón y Pacífico occidental).
Si bien México es considerado de baja endemicidad, ésta no es homogénea y los estudios de seroprevalencia en nuestro país indican tasas de 0.93% (0.45-1.42) en Cancún y 2.55% (1.79-3.16%) en el sur de la Ciudad de México.
La HB se transmite a través de contacto percutáneo o mucoso con sangre o líquidos corporales como semen, secreciones cervicales y saliva contaminados. La actividad sexual es el factor de riesgo más frecuente en pacientes con hepatitis B, sin embargo, la cobertura con vacuna contra hepatitis B entre adolescentes y adultos con prácticas sexuales de alto riesgo se reporta como bajo. De aquí la importancia de establecer programas de vacunación en el adolescente previo al inicio de la actividad sexual.
La OMS ha recomendado que todos los recién nacidos en el mundo reciban la vacuna contra hepatitis B, con una disminución significativa de la infección aguda y las complicaciones crónicas de la enfermedad.
El virus del papiloma humano (VPH) se asocia a papilomatosis laríngea en niños y a carcinoma cervical, anorrectal, vaginal y de cabeza y cuello en los adultos. Su adquisición muestra una distribución bimodal. En el primer año de la vida generalmente es el reflejo de una transmisión vertical, es muy probable que la infección sea asintomática y el virus se elimine en los siguientes años de vida o que la carga viral sea indetectable por los métodos de diagnóstico actuales. En otras ocasiones el niño puede desarrollar papilomatosis laríngea asociada a los tipos 6 y 11. Posteriormente la prevalencia de la infección por este virus aumenta en paralelo con el inicio de la actividad sexual en el grupo de adolescentes de 16 a 20 años de edad. La adquisición intrafamiliar es muy infrecuente.
En México en 2007 se notificaron 21 539 casos de cáncer genital. De todos los casos, 95% se presentan en mujeres, dentro de las cuales, 15 a 22% se presentan en el grupo de 20-24 años y 21 a 33% en el de 25-44 años. El papel causal de las infecciones por VPH en mujeres en el desarrollo de cáncer cervicouterino ha quedado documentado más allá de cualquier duda razonable. Existen alrededor de 120 tipos de VPH que infectan al ser humano, por lo menos 30 infectan el área genital, 15 son de alto riesgo de cáncer.
El virus del papiloma humano se encuentra ampliamente diseminado en el mundo e infecta tanto a hombres como a mujeres, se ha estimado que alrededor de dos tercios de las mujeres y de los hombres sexualmente activos han tenido infección por el VPH en algún momento de su vida.
El riesgo de infección por el VPH a través de los años es mayor al 50%, es la infección de transmisión sexual mas frecuente.
En el mundo el VPH16 se identifica en 50%; el VPH18 en 20%, el VPH45 en 8% y el VPH31 en 5%; algunos causan verrugas genitales y otros pueden provocar cáncer cervicouterino, del ano, pene, vagina y vulva. En México cerca del 75% del cáncer cervicourterino se asocia a los genotipos 16 y 18. El intervalo entre la infección y la progresión a malignidad es de aproximadamente 10 años.
Vacuna tetravalente recombinante que incluye a los tipos 6, 11, 16, 18 (Gardasil®).
Los estudios clínicos indican que tiene una eficacia del 100% en prevenir infección persistente por el virus del papiloma humano; previene lesiones de cáncer cervical, vaginal y vulvar, así como de verrugas genitales.
La vacuna se recomienda en un esquema de tres dosis administradas a los cero, dos y seis meses después de la primera dosis. La edad recomendada en el momento actual es hasta los 45 años por vía intramuscular.
Vacuna bivalente que contiene los serotipos 16 y 18 (Cervarix®). Tiene una eficacia de 98% en prevenir lesión intraepitelial grados 2 y 3 y adenocarcinoma in situ para los genotipos 16 y 18 cuando la vacuna se administra antes de la primera infección, y del 44% en mujeres con neoplasia intracervical o infección por VPH 16 y 18 previo a la administración de la vacuna. La vacuna confiere protección cruzada con otros tipos oncogénicos (VPH31 y VPH45).
Se aplica de los 10 a los 55 años de edad en un esquema de tres dosis a los cero, uno y seis meses posteriores a la primera dosis por vía intramuscular.
Esta vacuna obtuvo su registro en 2007 en el Reino Unido y en México.
En México están autorizadas las dos vacunas. En 2008 se incluyeron como parte del programa de inmunizaciones para mujeres que viven en poblaciones de alto riesgo para el desarrollo de cáncer cervicouterino.
Para las dos vacunas se aprobó también un esquema para las niñas menores de 14 años de dos dosis a los cero y seis meses, con adecuada protección y seguridad.
Vacuna nonavalente: Gardasil® 9 produce inmunización frente a lesiones precancerosas y cánceres que afectan al cuello de útero, vulva, vagina o ano debidas a siete tipos de alto riesgo (16, 18, 31, 33, 45, 52 y 58), y frente a verrugas genitales derivadas de los tipos 6 y 11 de VPH.
No sólo previene 90% de los cánceres de cuello de útero, sino que también se ponen en marcha programas efectivos de inmunización para otras enfermedades infecciosas relacionadas con el VPH, como es el cáncer anal, de vulva o vagina, para los cuales no existe un cribado sistemático.
En Mexico en 2018 y 2019 se notificaron a la Direccion General de Epidemiologia 8 027 y 9 806 casos de hepatitis A en toda la República Mexicana, que pudieran ser mayores debido al subregistro de esta enfermedad.
Es un virus de RNA no envuelto, perteneciente a la familia Picornaviridae; el humano es el único reservorio, la transmisión es principalmente fecal-oral, directa por contacto de persona a persona o indirecta a través de agua o alimentos contaminados; la transmisión por vía parenteral o sexual es rara, no se han documentado casos de transmisión por saliva o transmisión vertical.
Se han descrito cuatro patrones epidemiológicos de acuerdo a su endemicidad, que está directamente relacionada con las condiciones higiénicas y sanitarias del país. El patrón de endemicidad alto se caracteriza por afectar al grupo de preescolares, la transmisión es de persona a persona, la persistencia de la inmunidad es casi universal en adulto, casi nunca hay informes de epidemias. A los 10 años 90% de la población tiene anticuerpos contra el virus de la hepatitis A.
El patrón de endemicidad intermedio afecta principalmente a los escolares; la transmisión incluye alimentos y agua y los brotes epidémicos son comunes. A los 25 años de edad 80% de los individuos tienen anticuerpos contra el virus de la HA. El patrón de transmisión bajo afecta en especial a los adolescentes y adultos, también se relaciona con alimentos y agua contaminados, son frecuentes las epidemias. A los 50 años 80% tienen anticuerpos contra el virus de la HA. El patrón de transmisión muy bajo afecta principalmente a los adultos, los casos notificados se vinculan con brotes y antecedentes de viajes a regiones con alta transmisión, contacto con migrantes o ingesta de alimentos importados.
El patrón de endemicidad está relacionado con los hábitos de higiene y las condiciones sanitarias de cada área. En un mismo país estos patrones pueden variar. México es un país de endemicidad intermedia con variaciones que van desde baja hasta alta en las diferentes regiones geográficas.
Los estudios de seroprevalencia en México en 2006 indican 81% de seropositividad en los individuos de 16 a 20 años.
La expresión clínica de la infección por VHA es dependiente de la edad, con una mayor morbimortalidad a mayor edad; hasta en 70% de los menores de seis años son asintomáticos en contraste con los mayores de 16 años, en quienes la presentación con ictericia representa 70 a 95% de los casos. La forma sintomática en 10% de los casos puede evolucionar a hepatitis recurrente (reaparición de los síntomas, elevación de pruebas de función hepática y detección del virus en heces).
La hepatitis fulminante es la expresión más grave de la enfermedad, se presenta en 0.5 a 2% de los casos, se manifiesta en las siguientes ocho semanas posterior al inicio de la ictericia, con necrosis hepática masiva y una elevada mortalidad.
La tasa de mortalidad es de 0.3% y puede ser hasta de 2.69% en mayores de 49 años.
La vacuna contra la hepatitis A se recomienda a partir del año de edad, en un esquema de dos dosis, una inicial y otra adicional seis a 12 meses posteriores a la primera dosis.
La vacunación en niños y adolescentes se recomienda en regiones donde la incidencia es de 10-20 casos/100 000 habitantes y también en otros grupos como: pacientes con enfermedad hepática crónica, homosexuales, usuarios de drogas intravenosas, personas que conviven en hacinamiento, estudiantes en internados, orfanatos, cuarteles, en caso de brotes y contingencias como inundaciones y otros desastres naturales.
Actualmente están disponibles vacunas de virus inactivados, con una eficacia clínica similar (Avaxim Ped, Havrix, Vaqta) y una vacuna combinada hepatitis A y hepatitis B (Twinrix), esta última para personas de 18 años y mayores. En México esta vacuna no está incluida en el programa oficial de vacunación, pero está aprobada y disponible.
La administración de la vacuna en los cinco días siguientes al contacto tiene un elevado porcentaje de protección.
Es una enfermedad altamente contagiosa con distribución universal, causada por el virus de varicela-zóster (VVZ), cuya incidencia por grupos de edad varía con la localización geográfica. Puede presentarse desde la etapa del recién nacido con un pico máximo entre los tres y seis años de edad. Más de 90% de los casos ocurre antes de los 20 años de edad. Los casos secundarios se presentan hasta en 90% de los contactos susceptibles. La infección natural induce inmunidad probablemente de por vida, por lo que la recurrencia es extraordinariamente poco frecuente.
En México para la semana 52 del año 2019 se habían notificado a la Dirección General de Epidemiología 108 602 casos.
El virus de la varicela zóster es un virus de DNA, pertenece a la familia de los Herpes humanos tipo 3 y la subfamilia Herpes viridae alfa.
La infección por varicela es generalmente considerada una enfermedad benigna en niños inmunocompetentes, sin embargo, se puede asociar a complicaciones como infecciones de piel y tejidos blandos. En estos pacientes existe mayor riesgo de presentación de infecciones invasoras por Streptococcus beta hemolítico del grupo A (miositis, fascitis necrosante).
Los recién nacidos pueden presentar varicela en los primeros 16 días de vida cuando la mamá presenta lesiones activas durante el parto. Si la embarazada adquiere la infección en el primer o segundo trimestre de la gestación, en 1 a 2% de los casos se presenta la varicela congénita caracterizada por cicatrices cutáneas, atrofia de extremidades, coriorretinitis, catarata e hidrocefalia. No se ha descrito varicela congénita si la madre padece zóster durante el embarazo. Si la madre padece la enfermedad cinco días previos al parto o dos días después del mismo, se presenta la varicela perinatal en 15 a 30% de los recién nacidos con diseminación visceral y mortalidad de hasta 30%.
Los pacientes con padecimientos hematooncológicos y otros estados de inmunosupresión (postrasplante de médula ósea, hígado, riñón, etc.) pueden desarrollar varicela progresiva con diseminación visceral y mortalidad de 7 a 15%.
Después de la infección primaria, el VVZ queda latente en los ganglios de las raíces sensitivas dorsales y los ganglios de los nervios sensitivos craneales a donde llega fundamentalmente por vía retrógrada desde las vesículas cutáneas, este estado de latencia está regulado por mecanismos de la respuesta inmune celular. Años después el virus se puede reactivar dando como resultado el herpes zóster (HZ) que se caracteriza por la aparición de lesiones vesiculares dolorosas, que habitualmente siguen la distribución de un dermatomo; las complicaciones incluyen neuritis posherpética, encefalitis, ventriculitis y paresias.
Grupos de población que potencialmente pueden ser de mayor riesgo para complicación de varicela son: adolescentes de más de 14 años y adultos, embarazadas, menores de un año, recién nacidos de madres con varicela en el periodo neonatal, pacientes con inmunodeficiencias congénitas y adquiridas; tratamiento crónico con salicilatos, inmunosupresores y esteroides, personas con enfermedades cutáneas diseminadas y pulmonares crónicas.
La vacunación contra varicela está indicada en todos los individuos susceptibles. En México no está incluida en el programa oficial de vacunación pero las vacunas disponibles están aprobadas.
En 1974 Takahashi desarrolló en Japón una vacuna atenuada en fibroblastos de pulmón fetal humano, en embriones de cerdo de Guinea y en cultivo de células diploides humanas. En 1995 fue autorizada en Estados Unidos para uso sistemático a partir de los 12 meses de edad y posteriormente en algunos países de Europa y Asia. Es altamente inmunogénica, con una eficacia clínica del 95% y una inmunogenicidad aumentada al 99% con una segunda dosis, con persistencia de anticuerpos ocho a 20 años posteriores a la inmunización.
Los estudios demuestran que esta vacuna es bien tolerada, se presentan reacciones leves en 5 a 35% de los receptores (dolor y enrojecimiento en el sitio de aplicación). Entre el 5° y 26° días posvacunación se pueden presentar lesiones maculares o vesiculares localizadas o generalizadas similares al cuadro de varicela en 3 a 5% de los casos, fiebre de baja intensidad en el 15%, y mayor a 38 °C en el 10% de los receptores. La vacuna contra varicela puede administrarse en forma simultánea con otras vacunas como la triple viral pero en sitios diferentes; si esto no es posible el intervalo de administración debe ser no menor de un mes. Se recomiendan dos dosis. En mayores de 13 años la segunda dosis debe aplicarse con un intervalo de cuatro a ocho semanas.
Se dispone de dos vacunas con eficacia y perfil de seguridad similares: Varilrix® y Varivax®.
La administración de la vacuna contra varicela en susceptibles > 1 año de edad, en las primeras 72 h (hasta 120 h) después de la exposición puede prevenir o modificar el curso de la enfermedad.
La vacuna contra varicela no se encuentra en el Programan Nacional de Vacunación, sin embargo, las vacunas existentes están aprobadas y disponibles en nuestro país.
Evidentemente la tetravalente ofrece una mejor protección pues abarca cuatro cepas del virus, pero las dos son útiles. Su aplicación se recomienda en forma anual previa al inicio de la temporada invernal.
Se recomienda el uso de esta vacuna en países donde la enfermedad meningocócica es endémica, también en personas expuestas con enfermos comprobados de enfermedad meningocócica y en poblaciones “cerradas” como internados, asilos y cuarteles.
Se esperan en un futuro próximo nuevas vacunas para el adolescente y esto representará un reto más en la plataforma de vacunación para este grupo de edad. Las elevadas coberturas de vacunación en niños se han establecido a través de los años, por lo que el éxito en la implementación del esquema de vacunación en el adolescente requiere de tiempo, recursos, voluntad política, etcétera.
Desde hace muchos años se ha establecido que antes de aprobar el uso de alguna vacuna en humanos, debe quedar fehacientemente demostrada su eficacia y seguridad y haber superado distintas fases de estudios “preclínicos” en el laboratorio y en animales para posteriormente pasar a los estudios clínicos de la Fase I a la Fase III en voluntarios humanos adultos, donde se determina la dosis, la conveniencia o no de realizar refuerzos y periodicidad, pero principalmente se comprueba la seguridad al descartar la asociación causa-efecto de la vacuna en experimentación con eventos adversos serios, se registran los eventos adversos que pudieran esperarse con la vacunación, la mayoría de éstos suelen ser no serios, de corta duración y de evolución espontánea hasta su desaparición generalmente en las primeras 24 a 72 h posteriores a la aplicación de la vacuna, estos eventos adversos no serios asociados a la vacunación son, entre otros: fiebre, malestar general, cefalea, dolores musculares, disminución del apetito, dificultad para el sueño, dolor y enrojecimiento local en el sitio de aplicación de la vacuna.
En situaciones de “normalidad”, completar todas las etapas para contar con una vacuna aprobada suele requerir entre 10 y 15 años de trabajo por instituciones altamente especializadas y con gran experiencia.
En el caso particular de las vacunas contra la Covid-19, este proceso ha tenido una disminución importante en el tiempo, debido principalmente a que desde hace más de 10 años ya se habían iniciado los esfuerzos para contar con alguna vacuna contra otros tipos de coronavirus, lo que significó una gran diferencia y ahorro de tiempo, sin embargo, para la aprobación final de las vacunas se requiere haber concluido exitosamente la fase III, en donde siguiendo meticulosamente en el corto y largo plazos a los miles de voluntarios incluidos en los protocolos de investigación, queda demostrado que la vacuna no se asocia a eventos adversos serios y si resulta eficaz, mediante la medición de los anticuerpos séricos antes y después de la aplicación de la vacuna, se requiere que esta fase de la investigación se realice con sujetos que reciban la vacuna y otros un placebo en forma “ciega” para que ni el sujeto que la recibe ni el investigador sepan quiénes recibieron el placebo y quiénes el producto de investigación.
En casos especiales y cuidadosamente estudiados es posible obtener una autorización del uso de una vacuna antes de haber completado en su totalidad la fase III, como es el caso de la pandemia en que nos encontramos; esta autorización se obtiene con el propósito de controlar la pandemia lo más rápido que se pueda y en este caso en particular se autoriza para el uso de “emergencia” de la vacuna al completar y hacer un análisis parcial que garantice su seguridad al descartar la presencia de eventos adversos serios asociados a la vacuna durante varios meses.
El realizar estos estudios en poblaciones que sufren activamente la pandemia permite no solamente analizar la seguridad (no relación de la vacuna con eventos adversos serios) y la eficacia (a través de la evidencia de producción de anticuerpos protectores), sino la efectividad (con la demostración de la disminución estadística de presencia de casos durante el periodo de estudio en quienes recibieron la vacuna comparados con quienes recibieron placebo). Por razones éticas al finalizar el estudio, quienes recibieron placebo al demostrarse la utilidad de la vacuna deben ser vacunados gratuitamente para que se vean favorecidos igualmente con la protección que la vacuna ofrece.
De cualquier forma, la aprobación de las vacunas para su uso general (no solamente uso de emergencia), se podrá realizar cuando los estudios de fase III concluyan y eso no será posible antes de finales del 2021 o principios del 2022.
Por otra parte, siempre existe la posibilidad de que distintos grupos de población respondan de manera diferente a la vacuna, por lo que es conveniente que en esta fase III donde participan miles de sujetos, siempre que sea posible los estudios se realicen tomando en cuenta la participación de voluntarios de distintos países, razas, edades, etcétera.
En el caso particular de las vacunas contra la Covid-19, México ha participado en estudios de fase II y fase III de distintas vacunas, por lo que se conoce en forma estadística la respuesta de nuestra población ante los diferentes inmunógenos.
Una vez concluidos en forma satisfactoria los estudios realizados en voluntarios adultos, se inician estudios de eficacia y seguridad en población pediátrica. En la actualidad ya se han iniciado algunos estudios en menores, para ello deben cumplirse a cabalidad con todos los principios éticos tanto a nivel nacional como internacional.
La participación de los distintos países en esos protocolos de investigación clínica, les permite tener con mayor facilidad en forma temprana el acceso a las vacunas cuando éstas son aprobadas. México desde hace más de 15 años participa en forma activa en estos proyectos y ha recibido los beneficios de acceder a las vacunas casi al mismo tiempo que otros países con mayor desarrollo y poder económico que también participan en ellos, como ejemplo podemos mencionar distintas vacunas como: rotavirus, neumococo, virus del papiloma humano, entre otras.
La activa participación de distintos grupos de investigadores mexicanos le ha permitido al país acceder en forma temprana a diferentes vacunas contra la Covid-19.
Antes de poder aplicar las distintas vacunas, se requiere contar con la autorización de la OMS y de las “Agencias locales de cada país”, en México es la Cofepris (Comisión Federal para la Protección contra Riesgos Sanitarios).
Normalmente para obtener estas autorizaciones es necesario haber concluido con los estudios clínicos de fase III y que éstos hayan demostrado niveles adecuados de eficacia y seguridad. En el caso particular de la Covid-19, con la intención de interrumpir en la medida de lo posible la circulación natural del virus y limitar el impacto de la pandemia, en varios casos se ha logrado obtener la “autorización para uso de emergencia” de distintas vacunas. Para esto se toma en cuenta que los estudios clínicos de fase II hayan terminado, que se hayan demostrado adecuados niveles de eficacia y seguridad, y de que en el análisis de los avances de los estudios clínicos de fase III, no se hayan encontrado efectos adversos serios de impacto, asociados a la vacuna.
La autorización final podrá darse cuando concluyan de manera favorable los diferentes estudios de fase III.
Aunque la mayoría de los estudios de Fase III todavía siguen en curso, el poder vacunar a la población representa la mejor oportunidad para alcanzar el control de la enfermedad pandémica. Actualmente se cuenta con distintas vacunas para la prevención del Covid-19 (Cuadro 25).
| Cuadro 25. Vacunas para la prevención del Covid-19 | |||||
| Vacuna | Mecanismo de acción | Eficacia | Número de dosis | Temperatura conservación (°C) | Efectos secundarios |
| PFIZER BIONTHECH, | RNA mensajero, nanopartículas | Enf. general 94% Enf. grave 100% |
2 | -70 2–8 5 durante 5 días |
Síntomas locales, cefalea, fiebre, escalofríos, malestar general |
| MODERNA | RNA mensajero | Enf. general 94% Enf. grave 100% |
2 | -25 a -15 2–8 |
Síntomas locales, cefalea, fiebre, escalofríos, malestar general |
| ASTRA ZÉNECA | Vector viral | Enf. general 70% Enf. grave 100% |
2 | 2–8 | Síntomas locales, cefalea, fiebre, escalofríos, malestar general |
| JOHNSON & JOHNSON | Adenovirus 26 | Enf. general 72% Enf. grave 85% |
1 | -20 2-8 |
Síntomas locales, cefalea, fiebre, escalofríos, malestar general |
| NOVAVAX | Subunidad proteica | Enf. general 89% Enf. grave ¿? |
2 | 2–8 | Síntomas locales, cefalea, fiebre, escalofríos, malestar general |
| GAMALEYA | Adenovirus 26-5 | Enf. general 91% Enf. grave 100% |
2 | 18 líquida 2–8 |
Síntomas locales, cefalea, fiebre, escalofríos, malestar general |
| SINOPHARM | Virus inactivado | Enf. general 79 - 86% Enf. grave ¿? |
2 | 2–8 | Síntomas locales, cefalea, fiebre, escalofríos, malestar general |
| CANSINO | Adenovirus 5 | Enf. general 76% Enf. grave 92% |
1 | 2–8 | Síntomas locales, cefalea, fiebre, escalofríos, malestar general |
| CUREVAC | RNA mensajero | En desarrollo | 2 | 2–8 | Síntomas locales, cefalea, fiebre, escalofríos, malestar general |
El tener acceso oportuno a las vacunas no garantiza que la población quede inmunizada, ya que se requiere de muchos otros aspectos que incluyen:
Finalmente, el contar con un número importante de personas vacunadas a nivel global permite prever que se ha avanzado para el control de la epidemia, sin embargo, será necesario seguir avanzando para vacunar al mayor número posible de personas en México y en todo el mundo; queda pendiente el tener información confiable sobre la conveniencia o no, de la necesidad de aplicar refuerzos de la vacuna, lo que será necesario una vez que se determine en qué condiciones de tiempo deberán aplicarse, siendo posible que sea diferente para cada vacuna y, por otra parte, el seguimiento sobre la posible aparición de mutaciones en el virus que pueden dar origen a modificaciones en la enfermedad y en el efecto de las vacunas para su prevención.
El personal de salud está mayormente expuesto a contraer infecciones debido al contacto cercano y frecuente de personas enfermas, las medidas de prevención para evitarlo incluyen como parte fundamental la inmunización.
En los procesos de vacunación debe incluirse a todo el personal de salud (médicos, enfermeras, personal de laboratorio, técnicos, terapistas, estudiantes, personal voluntario, personal de seguridad, personal de intendencia, etc.).
Se recomienda que todo el personal que labore en instituciones de salud haya recibido inmunización contra: sarampión, parotiditis, rubéola, varicela, Pertussis, hepatitis B, influenza (anual al inicio de la temporada invernal). En situaciones especiales debe recibir otras vacunas: zóster, meningococo, neumococo, rabia, etc.
Durante la temporada de influenza, este padecimiento representa el mayor riesgo de contagio para el personal de salud.
Los beneficios que se persiguen al vacunar al personal de salud son, entre otros:
Se dispone de algunas vacunas para poblaciones específicas, principalmente para ser aplicadas en algunas regiones y en poblaciones endémicas y/o en situaciones específicas como: fiebre amarilla, dengue, etc.
Actualmente se encuentran en investigación al menos cuatro nuevas vacunas contra Chlamydia trachomatis, citomegalovirus, Herpes simple tipo 2 y Streptococcus del grupo B, cuya población destinataría más importante es la de adolescentes; contar con estos inmunógenos representará un beneficio adicional a los esquemas actuales.
Otras vacunas en estudio a nivel internacional son contra paludismo, VIH, virus sincicial respiratorio, además de que siguen en estudio vacunas contra dengue, entre otras.
Lo más importante es entender y aceptar que la vacunación es un procedimiento seguro y eficaz, de gran valor y utilidad, no solamente para los niños, sino para los adolescentes, los adultos y para grupos específicos de población.
Desde hace aproximadamente 15 años la OMS declaró que la vacunación es una de las maniobras con mayor costo-efectividad y mayor costo-beneficio en salud, solamente comparable con el agua potable.