Figura 1
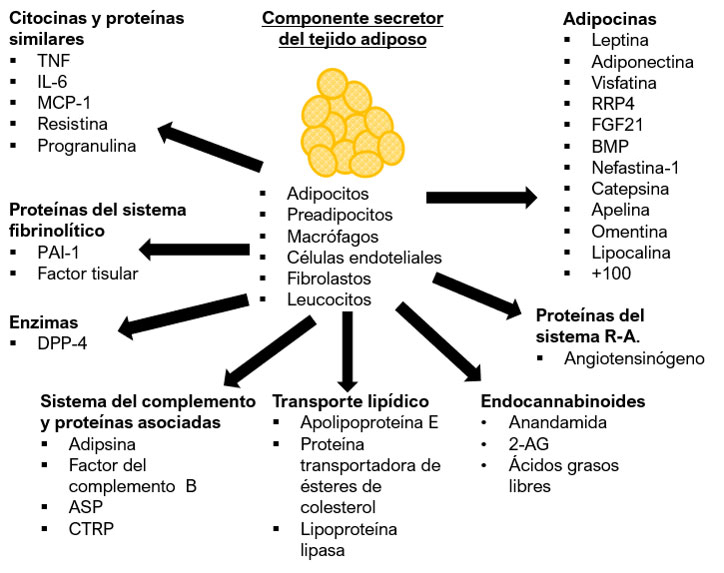
Sustancias secretadas por el tejido adiposo. Modificado de: Luo L, Liu M. "Adipose tissue in control of metabolism" J ENdocrinol. 2016; 231(3) R 77-99.
Coordinador: Dr. Miguel Ángel Rodríguez Weber
Obesidad: complicaciones en la infancia y en la adolescencia
Aspectos epidemiológicos, clínicos y terapéuticos subestimados
Dr. Arturo Perea Martínez
La obesidad es una enfermedad sistémica, crónica, inflamatoria, recurrente, que impacta negativamente en la salud, el bienestar y la productividad individual y colectiva. Por su creciente prevalencia en todo el mundo y en particular en México, se ha convertido en uno de los problemas de salud más importantes en nuestro tiempo.
A la par con su ascendente prevalencia, la aparición de complicaciones sistémicas asociadas a la obesidad es también cada vez más frecuente y en edad más temprana. Así, enfermedades como la dislipidemia aterogénica (DAT), la diabetes mellitus tipo 2 (DM2), la hipertensión arterial sistémica (HTA), la enfermedad hepática grasa no alcohólica (EHGNA) y el síndrome de apnea obstructiva de sueño (SAHOS), entre otras, alcanzan cifras de afectación muy preocupantes, deterioran el bienestar y contribuyen al impacto que la obesidad genera en el individuo, en la familia y en la colectividad.
A continuación, algunos conceptos generales poco profundizados en la práctica asistencial de la obesidad en la infancia y la adolescencia, en particular con enfoque al desarrollo de enfermedades no transmisibles en la infancia y en la adolescencia, y la oportunidad de prevenirlas y en su caso contener la evolución.
En 2018 la Organización Mundial de la Salud (OMS) reportó cerca de 2 billones de adultos de 18 años, 650 millones de ellos padecían obesidad. En niños y adolescentes, 41 millones de niños menores de cinco años de edad y hasta 340 millones de niños y adolescentes padecían sobrepeso y obesidad.
Las recomendaciones de la Comisión para acabar con la obesidad infantil, emitidas en 2016 y adoptadas por la OMS, incluye seis estrategias:
La misma Comisión sugiere las siguientes acciones:
En México, la Encuesta Nacional de Salud y Nutrición de 2018 describe una prevalencia nacional de sobrepeso en menores de cuatro años de edad, la cual es de 8.2%.
En niños de cinco a 11 años de edad, la prevalencia del sobrepeso es de 18.1% y de obesidad 17.5%. El resultado total de ambas condiciones alcanza 35.6%, con una distribución de 37.9% en el área urbana y 29.7% de la rural.
En el grupo de adolescentes de 12 a 19 años de edad, la prevalencia de sobrepeso/obesidad reportada es del 38.4%, predominando en mujeres (41.1%).
En adultos de más de 20 años, 75.2% presentan sobrepeso u obesidad.
La Clínica de Obesidad y Enfermedades No Transmisibles en el Instituto Nacional de Pediatría (COyENT-INP), destaca los siguientes aspectos:
México ha dado una respuesta con la creación y desarrollo de la Estrategia Nacional para la prevención y control del sobrepeso, la obesidad y la diabetes (ENPSOD). Incluye tres ejes de acción: el primero la salud pública. El segundo la atención médica. El tercero es el de la regulación sanitaria y política fiscal, que considera el etiquetado de los alimentos, su publicidad y las medidas fiscales.
En 2015, el Gobierno federal mexicano creó el Observatorio Mexicano de Enfermedades No Transmisibles (OMENT), un grupo multidisciplinario y multisectorial responsable de asentar y hacer valer el desarrollo de las acciones de la estrategia.
Acorde con reportes de la COyENT-INP, seis de cada 10 individuos presentan algún indicador clínico o bioquímico de una o más complicaciones relacionadas con la obesidad. Treinta y ocho porciento de los niños y adolescentes presentan síndrome metabólico (SM), dislipidemia aterogénica, 25% hipertensión arterial (HTA); 20% glucemia ≥ a 100 mg/dL; 22% elevación de enzimas hepáticas sin una causa diferente a la obesidad; 22% padecen hiperuricemia; 44% repercusión psicosocial; 22% afectación musculoesquelética, y 40% alguna expresión de afectación ventilatoria.
Tejido adiposo. Como tejido adiposo (TA) se denomina al agregado celular de adipocitos, preadipocitos, macrófagos, células endoteliales, fibroblastos y leucocitos; reconocido por sus importantes funciones en la regulación del metabolismo sistémico. El tejido adiposo en normalidad realiza funciones que determinan el mantenimiento de la homeostasis sistémica, destacando el almacenamiento de triglicéridos bajo condiciones de exceso calórico y su liberación durante los periodos de ayuno, la termorregulación y la protección de órganos.
Se clasifica en tejido adiposo blanco (TAB) y tejido adiposo pardo (TAP), los cuales tienen características funcionales y morfológicas diferentes. El TAB se compone principalmente de células uniloculares (constituido por una gran gota de grasa), con una elevada capacidad para almacenar triglicéridos, mientras que el TAP o tejido multilocular contiene adipocitos con múltiples gotas pequeñas de grasa; estos adipocitos son ricos en mitocondrias. Morfofuncionalmente, el tejido adiposo en el cuerpo humano contiene dos amplios depósitos, el tejido adiposo visceral (TAV) y el tejido adiposo subcutáneo (TAS).
Estas clasificaciones son útiles para diferenciar los efectos de un desbalance en las concentraciones de este tipo de tejidos, debido a que se ha identificado un vínculo entre el incremento del TAV y riesgo cardiometabólico, en oposición al perfil neutral o incluso cardioprotector asociado a las elevaciones del TAS.
Adipocinas. En los últimos decenios se ha demostrado que el TA cuenta con importantes funciones autocrinas, paracrinas y endocrinas. Produce un vasto número de sustancias que regulan el metabolismo ejerciendo funciones benéficas y necesarias para mantener un adecuado estado de salud, interviniendo en procesos vitales como la secreción de insulina, la regulación del hambre y la saciedad y en el equilibrio energético. Sin embargo, un incremento en los niveles de adiposidad central y en la síntesis de diferentes sustancias de orden proinflamatorio explica el origen del componente de inflamación que caracteriza al sobrepeso y a la obesidad, estas sustancias son denominadas adipocinas.
El impacto negativo del sobrepeso y la obesidad sobre la salud se encuentra íntimamente ligado a las altas cantidades de TAB que se depositan primordialmente en la región visceral, condicionante que contribuye al aumento del diámetro abdominal. El conocimiento de las adipocinas y sus efectos sistémicos supone uno de los principales mecanismos fisiopatológicos que culminan con la manifestación de alteraciones metabólicas sistémicas y daño endotelial, existiendo una fuerte asociación entre este último y el desarrollo de enfermedades cardiovasculares (Figura 1).
Figura 1

Sustancias secretadas por el tejido adiposo. Modificado de: Luo L, Liu M. "Adipose tissue in control of metabolism" J ENdocrinol. 2016; 231(3) R 77-99.
La hipertrofia de los adipocitos propia del exceso de tejido adiposo se asocia fuertemente a la elevación de adipocinas con efectos proinflamatorios, entre éstas se incluyen la leptina, IL-6, IL-8 y proteína quimiotáctica de monocitos 1 (MCP-1), aunado a la disminución de niveles reducidos de la adiponectina (adipocina relacionada con la sensibilidad a la insulina) y la IL-10, que tiene un efecto antiinflamatorio casi total (Figura 2).
Figura 2
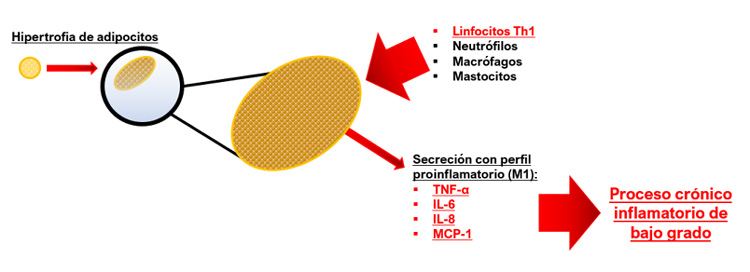
Cascada de secreción proinflamatoria en el tejido adiposo.
En la obesidad, el TA se encuentra infiltrado por poblaciones crecientes de células inflamatorias como linfocitos (de manera predominante Th1), neutrófilos, macrófagos y mastocitos, mientras que las concentraciones de eosinófilos, las células Th2 y las células T-reg permanecen constantes o inclusive disminuidas.
Tejido muscular. El músculo es un tejido de origen mesodérmico que tiene como propiedad fundamental la contractilidad. La función principal atribuida al músculo es la locomoción, además, este tejido da estructura y es útil en la termorregulación del cuerpo. La OMS y otros organismos internacionales señalan que la actividad física regular representa un medio eficiente para prevenir y tratar diversas enfermedades no transmisibles como la diabetes mellitus, las enfermedades cardiovasculares, neurodegenerativas, pulmonares y algunas formas de cáncer, aunque los mecanismos mediante los cuales se obtienen estos efectos no se precisan. Por otra parte, la fisiopatología subyacente a la inactividad física está relacionada directamente con la acumulación de grasa visceral en el cuerpo, que provoca el inicio de una inflamación sistémica que complica la obesidad (Cuadro 2).
| Cuadro 2. Comparativa entre los efectos de la actividad y la inactividad física | |
| ACTIVIDAD FÍSICA | INACTIVIDAD FÍSICA |
| Mejora la sensibilidad a la insulina | Reduce sensibilidad a la insulina |
| Mejora el metabolismo | Pérdida muscular |
| Reduce la tensión arterial | Obesidad |
| Reduce el tejido adiposo | Diabetes mellitus tipo 2 |
| Reduce la inflamación | Síndrome metabólico |
| Mejora cardiorrespiratoria | Enfermedades mentales (demencia y depresión) |
| Reduce lípidos circulantes | Enfermedades cardiovasculares |
| Mantiene masa muscular | Cáncer de colon |
| Mejora el flujo de sangre al cerebro | Cáncer de mama posmenopáusico |
| Mejora la termorregulación | Cáncer pancreático, hepático y endometrial |
| Reduce la grasa visceral | Cáncer renal |
| Adenocarcinoma esofágico | |
| Osteoporosis y osteoartritis | |
| Disfunción eréctil | |
| Síndrome de ovario poliquístico | |
| Modificado de: Lula S, Ghafoor S. Myokines: Discovery challenges and therapeutic impediments. J Pak Med Assoc. 2019;69:1014-1017. | |
Mioquinas (miocinas). El concepto de miocinas es relativamente nuevo y se introdujo por Pedersen en el año 2003. Hace alusión a las citocinas producidas y liberadas por las fibras musculares, que ejercen efectos endocrinos, paracrinos y autocrinos, desde entonces la lista de miocinas descubiertas ha ido en ascenso día con día. Desde el momento de la detección del aumento en la expresión de interleucina 6 (IL-6) en biopsias musculares humanas obtenidas después del ejercicio y la liberación concomitante de esta IL-6 derivada del músculo a la circulación, se ha destinado especial atención a la búsqueda de otras citocinas procedentes de este tejido. En pruebas experimentales se ha promovido la producción y secreción de diversas miocinas posterior al ejercicio en músculo humano, detectando un incremento en los niveles intersticiales y séricos de IL-6, IL-8, IL-10, IL-15, ligando CC-quimiocina (CCL) 2, receptor IL-1 antagonista, calprotectina S100A9, y factor de crecimiento endotelial vascular (VEGF).
El aumento de la expresión y liberación de IL-6 y de otras citocinas ocurre independientemente del daño muscular; además, está regulado por la disponibilidad de carbohidratos y se propone que funge como sensor del estado metabólico del músculo. Un estudio reciente en roedores muestra que la liberación de la hormona osteocalcina derivada del hueso induce parte del aumento de IL-6 por ejercicio y una mayor capacidad de oxidación del sustrato.
Las células satélites, los fibroblastos, las células endoteliales y los macrófagos que residen en el tejido muscular contribuyen con la abundancia muscular y la liberación de proteínas (Figura 3) y sus diversas funciones (Cuadro 3).
Figura 3
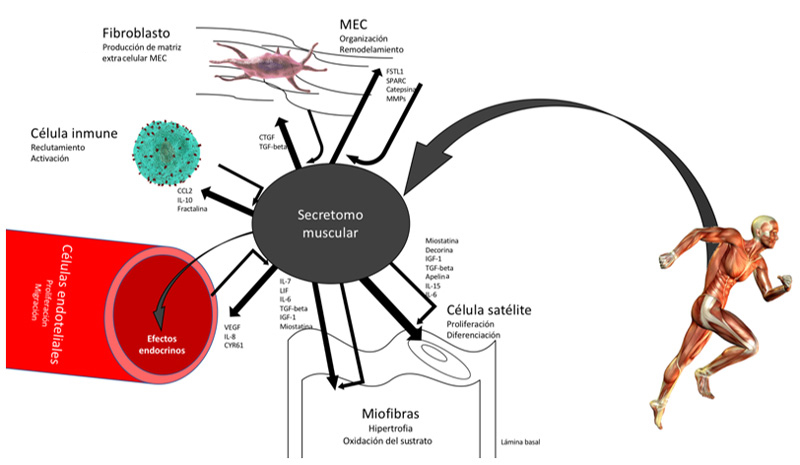
Efectos autocrinos y paracrinos de las miocinas humanas reguladas por el ejercicio. El efecto de las miocinas estimula e inhibe diversas funciones. [CTGF, factor de crecimiento del tejido conectivo; TGF-b, factor de crecimiento transformante b; IL, interleucina; MMP, matriz de metaloproteinasas; VEGF, factor de crecimiento endotelial vascular; SPARC, proteína secretada rica en cisteína; FSTL1, tipo follistatina 1; LIF, factor inhibidor de leucemia; IGF-1, factor de crecimiento similar a la insulina 1.] Modificado de: Hoffmann C, Weigert C. Skeletal muscle as an endocrine organ: The role of myokines in exercise adaptations. Cold Spring Harb Perspect Med. 2017;17:1-22.
| Cuadro 3. Miocinas y sus funciones | |
| ACTIVIDAD FÍSICA | INACTIVIDAD FÍSICA |
| Control del mecanismo de reparación tisular | Proliferación y migración de células satélite |
| Control de la cascada inflamatoria | Organización de la matriz extracelular |
| Influencia en el mecanismo de adhesión celular | Desmontaje de la matriz extracelular |
| Desarrollo anatómico estructural | Regulación positiva de la locomoción |
| Regulación de la angiogénesis | Modulación de la desgranulación de plaquetas |
| Efecto sobre la respuesta inmune del huésped | Regulación de la oxidación de ácidos grasos |
| Control de la secreción de insulina | Mecanismo de defensa antitumoral |
| Modificado de: Lula S, Ghafoor S. Myokines: Discovery challenges and therapeutic impediments. J Pak Med Assoc. 2019;69:1014-1017. | |
En la Figura 4 se describen las principales funciones de algunas de las miocinas y sus efectos sobre diversos tejidos.
Figura 4
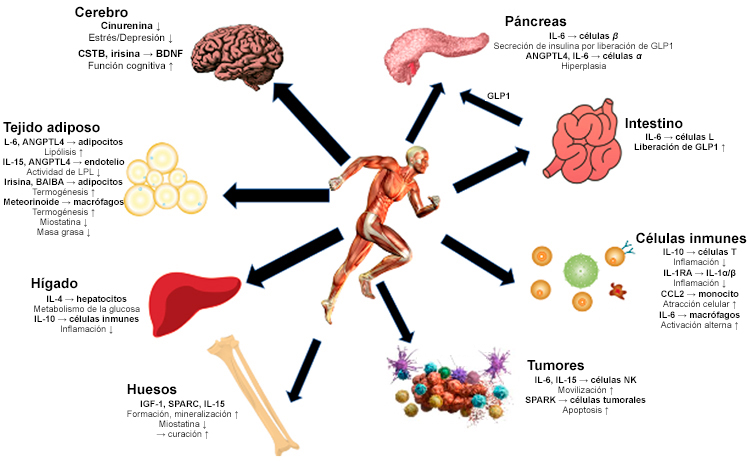
Efectos endocrinos de las miocinas y metabolitos humanos regulados por el ejercicio. Modificado de: Hoffman C, Weigert C. 2017. Skeletal muscle as an endocrine organ: the role of myokines in exercise adaptations. Cold Spring Harb Perspect Med. 2017;17:1-22.
Estudios recientes han demostrado que las miocinas tienen un efecto de regulación sobre las adipocinas, además de influir directamente en el TA mediante un aumento de la lipólisis y la termogénesis en los adipocitos, disminución de la actividad de la lipoproteína lipasa en el endotelio y aumento de la termogénesis con una sucesiva disminución de la miostatina y la grasa corporal (Figura 5).
Figura 5
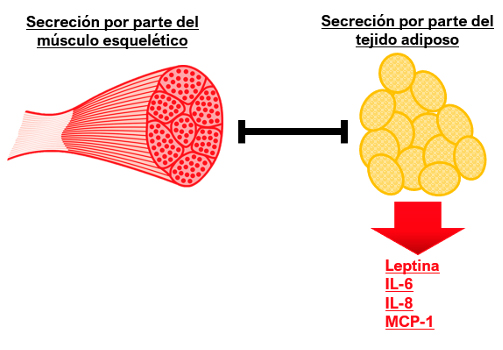
Interacción adipomiocina. Modificado de: Lizuka,K., Machida, T., & Hirafuji, M. (2014). Skeletal muscle is an endocrine organ. Journal of pharmacological sciences, 125(2), 125-131.
Etiología. La obesidad tiene diferentes causas, entre las cuales resalta la nutricional o exógena siendo 95% de los casos, y la endógena u orgánica 5% (4% asociada a síndromes dismórficos y 1% a enfermedades endocrinas).
Cuatro parámetros orientan a determinar la causa de la enfermedad: el fenotipo, la talla, el neurodesarrollo y la edad ósea (Cuadro 4). El fenotipo normal con talla normal o elevada, con neurodesarrollo normal y edad ósea normal o acelerada nos habla de obesidad nutricional o exógena. El fenotipo alterado y talla baja, sugiere síndromes o endocrinopatías.
| Cuadro 4. Obesidad. Diagnóstico etiológico | ||
| Obsesidad Exógena | Obesidad Endógena | |
| Fenotipo | Normal | Alterado |
| Talla | Normal o elevada | Baja |
| Neurodesarrollo | Normal | Alterado |
| Edad ósea | Normal o acelerada | Retrasada o acelerada |
La somatometría tiene un papel importante en la clasificación y diagnóstico de la obesidad y sus complicaciones, a través de la toma de índices como lo son la talla, el peso, la circunferencia de cintura, el cuello, el porcentaje de grasa y la tensión arterial, que a su vez forman indicadores para dar una acertada interpretación de los resultados, aquí se incluye el peso para la talla (en menores de cinco años), índice de masa corporal (IMC) para la edad (mayores de cinco años), índice cintura-estatura (ICE), porcentaje de grasa corporal y tensión arterial para la edad.
Los criterios internacionales señalan que para diagnosticar sobrepeso u obesidad en niños menores de dos años se utilicen las gráficas de la OMS y para mayores de dos años de edad utilizar las de los Centers for Disease Control and Prevention de Estados Unidos. La recomendación para establecer el diagnóstico es utilizar la puntuación z (z score) con puntos de corte que brinda la OMS.
El ICE sirve para determinar obesidad central (TAV) y se asocia con alteraciones sistémicas. El ICE en comparación con el IMC y la circunferencia de la cintura en forma aislada tienen mayor relación con riesgo de ECV. El ICE podría ser un buen predictor para el síndrome metabólico y el SAHOS. Por arriba de ≥ 0.50 se considera de riesgo. Estudios recientes demuestran una asociación entre EHGNA, los niveles de lípidos en sangre, el perfil hematológico y la presión arterial con la cintura y el ICE.
La COyENT realizó un estudio (n: 698) para evaluar la asociación entre el ICE estratificado en diferentes puntos de cohorte ascendentes con alteraciones sistémicas. En los resultados se observó que las alteraciones metabólicas mostraron una prevalencia de más de 50% en todos los estratos del ICE, las alteraciones hepáticas por encima del 48% en todos los estratos y la presión arterial, la prevalencia fue inferior a 40%.
La circunferencia de cuello (CCu) es un indicador de alerta de riesgo cardiovascular y de resistencia a la insulina. El TAS de la parte superior del cuerpo desempeña un papel en el riesgo cardiometabólico. Acorde con algunos estudios tiene mejor correlación que el IMC y la circunferencia de la cintura (CC) con acantosis nigricans, hiperglucemia, hiperuricemia y otros factores metabólicos. En la COyENT, la CCu comparativamente con el ICE, demostró ser un indicador clínico igualmente útil para la búsqueda de anormalidades bioquímicas en niños y adolescentes con obesidad. Es un procedimiento de medición menos invasivo, útil en circunstancias en las que el individuo no puede estar de pie, no es consciente, presenta alguna anomalía, o una condición abdominal u otra entidad que dificulte la medición de la circunferencia de la cintura y por lo tanto del ICE.
La utilidad e impacto de los índices e indicadores clínicos además de servir para el diagnóstico de obesidad, facilitan la detección y manejo de sus complicaciones.
Las causas que originan a la obesidad y las enfermedades no transmisibles (ENT) son de orden prenatal y posnatal.
La malnutrición de ambos padres (desnutrición, obesidad, carencias nutricionales específicas) antes de la concepción y de la madre durante la gestación, puede impactar en el desarrollo del feto y del recién nacido. La hipótesis del Dr. David Barker permitió reconocer la importancia de la vida fetal en el origen de la enfermedad cardiovascular, de la obesidad y otras enfermedades.
La programación es un proceso en el que las células se desarrollan, funcionan y se adaptan al medio ambiente en respuesta a un conjunto establecido de comandos ejecutables, a menudo provenientes de la cromatina de la célula, de tal manera que se entiende como “un proceso fetal de adaptación del crecimiento y función celular, orgánica y sistémica, en respuesta a uno o varios estímulos de diversa índole, que sujeta al producto a desarrollar modificaciones que pueden preservarse en la vida posnatal, predisponiéndole al riesgo de enfermedad y muerte temprana”.
La obesidad y las ENT ocurren como un fenómeno de programación multifactorial en donde una disrupción ambiental prenatal o posnatal (malnutrición), produce cambios epigenéticos que generan una respuesta adaptativa predictiva (programación) con efectos intergeneracionales en el genotipo y fenotipo al nacer, que influenciarán el fenotipo adulto y su predisposición a enfermedades como la obesidad, DM2, HTA, ECV, EHGNA y algunas formas de cáncer.
Los cambios epigenéticos resultan de factores de diversa índole que tienen la capacidad de modular la expresión genética de un individuo sin alterar la estructura base de sus genes, influyendo así en la conformación del fenotipo. La epigenética es mediada por trastornos de metilación del DNA, en la conformación de histonas, por micro-RNA y nc-RNA, así como por sirtuinas.
En la historia de la humanidad se han presentado exposiciones ambientales extremas en orden nutricional que han impactado en generaciones (Cuadro 5).
| Cuadro 5. Hambrunas relacionadas con el proceso de programación de la obesidad y las enfermedades no transmisibles | |||
| Nombre | País | Periodo | Exposición |
| Hambruna holandesa | Holanda | 1944 | Ingesta energética de 400 a 800 kcal al día |
| Asedio de Leningrado | Rusia | 1941 – 1944 | Ingesta energética de 300 kcal al día (más severo de 1941-1942) |
| Ocupación de Guernsey | Islas del Canal, Reino Unido | 1940 – 1945 | Ingesta energética de 1 200 kcal al día |
| Gran hambruna China (3 años amargos) | China | 1959 - 1961 | Variabilidad extrema entre las comunidades rurales y urbanas |
| Hambruna de Corea del Norte (ardua marcha) | Corea del Norte | 1994 – 1998 | Sin datos exactos |
Una de las exposiciones ambientales extremas más estudiadas es la hambruna holandesa, en la cual la exposición a una malnutrición materna durante la gestación predispuso a la descendencia al desarrollo temprano de enfermedad coronaria, hipertensión arterial y obesidad en la etapa adulta (Cuadro 6).
| Cuadro 6. Compilación de la predisposición a enfermedades en adultos con el trimestre del embarazo afectado por la hambruna holandesa | ||
| Primer trimestre | Segundo trimestre | Tercer trimestre |
| Enfermedad de la arteria coronaria | Enfermedad pulmonar | Diabetes |
| Hipertensión | Enfermedad renal | Depresión |
| Dislipidemia | Esquizofrenia | |
| Obesidad | Desorden de personalidad antisocial | |
En el caso de la hambruna de China se observa que los adultos de la primera generación que sobrevivieron en el útero, presentaron una disminución en la estatura y alteraciones en el desarrollo del sistema nervioso, asimismo, los nietos de la segunda generación presentaron un peso mayor al normal al nacer.
Condiciones de estrés oxidativo pueden llevar la modificación de la expresión genética embrionaria en periodos críticos del desarrollo. En el embarazo puede producirse por el consumo de tabaco, hipertensión/preeclampsia, inflamación/infección, obesidad y malnutrición, lo que conlleva a una modulación directa de la expresión genética y/o daño directo de las membranas celulares y otras moléculas en un momento crítico del desarrollo.
Partiendo de la salud de los gametos masculinos y femeninos, el ambiente fetal de la madre durante la gestación y las condiciones del mismo, pueden impactar a nivel intrauterino en el tamaño y morfología de estructuras y tejidos, irrigación sanguínea, oxigenación y el balance de perfusión placentaria, el transporte de nutrimentos puede verse aumentado, mayor producción de insulina, leptina y cortisol, producción de factores de crecimiento alterados, producción de citocinas como adiponectina, TNF-alfa, IL-6, entre otras, metabolismo alterado, etc., dando como resultado un impacto en el peso al nacer, la composición corporal, repercusiones metabólicas y alteraciones en el desarrollo del tejido adiposo, hígado, cerebro, páncreas y corazón (Figura 6).
Figura 6
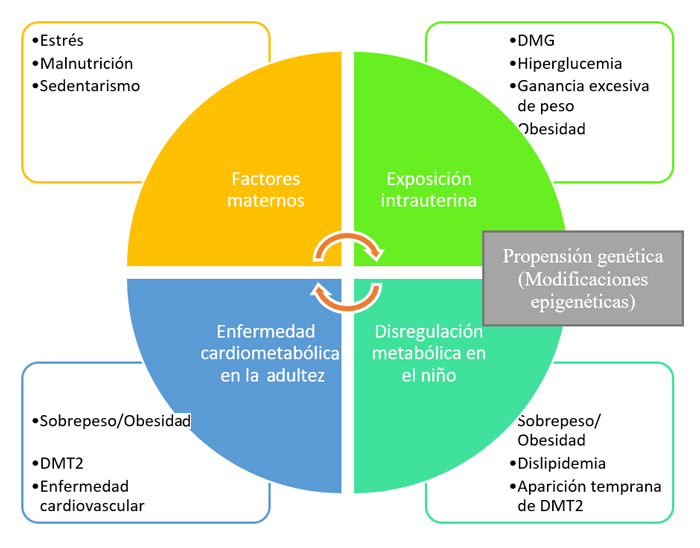
Proceso de programación sistémica.
La hipótesis de los orígenes tempranos de las enfermedades no transmisibles parece transitar hacia el desarrollo de éstas en la etapa fetal. En bebés de madres con hipercolesterolemia crónica o temporal se observan estrías de grasa en aortas de sus fetos. Además, infiltración de macrófagos, oxidación de colesterol LDL y desarrollo de células espumosas.
Respecto a la enfermedad hepática grasa no alcohólica (EHGNA), la gestante con sobrepeso, ganancia excesiva de peso, inflamación, exceso de lípidos y glucosa, condicionan resistencia a la insulina y que aumente el flujo placentario al feto. También se presume la transferencia del microbioma materno al neonato y el efecto de una placenta en el contexto de inflamación sistémica. Algunos autores presumen que en la gestación el feto muestra ya acumulación de grasa hepática que condiciona daño oxidativo, disfunción mitocondrial (sirtuinas), cebado de células Kupffer y cambios epigenéticos, que en un ambiente posnatal de riesgo (dieta rica en grasa y azúcares refinados) induce mayor acumulación de grasa en el hígado, mayor lipogénesis de novo (SREBP1C) y menor oxidación de ácidos grasos (PPAR-alfa), promoviendo daño hepatocelular con activación de las células Kupffer y estrelladas, apoptosis de hepatocitos, daño oxidativo y estrés en el retículo endoplasmático, liderando todo esto fácilmente a inflamación, daño hepático, esteatohepatitis y fibrosis.
En otros estudios se observa que la obesidad gestacional aumenta el riesgo de aparición de complicaciones asociadas con el embarazo en la mujer y su producto (Cuadro 7).
| Cuadro 7. Impacto de la obesidad en el binomio | ||||
| Riesgo | Normal | Obesidad | Obesidad Grave | |
| Mamá gestante | HTA | 1.8 (1.1-2.9) | ||
| Preeclamsia | 2.47 (1.66-3.67) | |||
| Diabetes | 3.56 (3.05-4.21) | 8.56 (5.07-16.04) | ||
| Cesárea | 20.7% | 33.85% | 47-4% | |
| Aborto/muerte fetal | 2.4-3.1 | |||
| Bebé | Anomalías congénitas | 1.7 DTN Cardiopatías/orofaciales, etc. |
3.0 (DTN) > IMC 7% Cardiopatías/orofaciales, etc. |
|
| Peso bajo | 10% | 18.8% | ||
| Peso alto | > IMC mat. | 2.0 (1.4-3.0) | 2.4 (1.5-3.8) | |
| Premadurez | < 32 sem. | 0.73 (0.65-0.82) | 2.13 (1.13-4.01) | |
La obesidad gestacional, al ocasionar estrés oxidativo e inflamación, induce disfunción mitocondrial y condiciona un impacto epigenético sobre la información del DNA. La hiperleptinemia e hiperinsulinemia ocasionan anormalidades en la interconexión de los núcleos que conforman el circuito del hambre y la saciedad, predisponiendo a la hiperfagia y alto nivel de saciedad lo que facilita el desarrollo de obesidad y ENT.
La malnutrición materna genera estrés de la función del eje hipotálamo-hipófisis-suprarrenales, lo que a largo plazo se asocia con crecimiento fetal disminuido.
En el feto, como en el recién nacido de peso bajo, los niveles de leptina son bajos, lo que se asocia con el incorrecto desarrollo de vías neuronales regulares, posible factor que facilita un consumo excesivo de alimentos en la vida extrauterina.
La insulina accede rápido al hipotálamo por medio de un proceso mediado por un receptor saturable y la difusión hacia la eminencia media, lo que regula la respuesta anorexigénica hipotalámica a través de la vía tirosincinasa unida a membrana, la cual a su vez, activa la cascada de señalización de PI3K (fosfatidil inositol 3 cinasa). Los receptores de insulina se expresan ampliamente en el cerebro debido a que esta es necesaria para el crecimiento neuronal. En estudios experimentales, la restricción nutricional durante la gestación dio como resultado retraso en el crecimiento intrauterino además de disregulación hipotalámica en la señalización y respuesta a insulina y leptina, limitando la respuesta anorexigénica.
En cuanto a las preferencias alimentarias, existe una programación hipotalámica tanto en la vida prenatal, facilitado por el tipo de dieta materna, como en la vida posnatal, impactando en áreas cerebrales como el núcleo accumbens, que inducen adherencia a sabores y conducta alimentaria de riesgo. Este conjunto de experiencias forman el escenario de nuestras elecciones de alimentos en el futuro y son importantes para el establecimiento de los hábitos alimentarios a largo plazo.
Influencia de los nutrimentos en el desarrollo de la obesidad y las ENT. El papel de las proteínas en la programación metabólica temprana, radica en las observaciones que asocian a la lactancia materna exclusiva con menor riesgo de desarrollar obesidad en la infancia y más adelante en la vida adulta. La diferencia en el contenido de proteínas entre la leche humana y las fórmulas lácteas infantiles, ha generado la hipótesis de la proteína temprana. Una revisión se centra en un enfoque mecanicista de la adiposidad programada y el crecimiento y desarrollo de otros órganos mediante la ingesta de proteínas en la infancia, que puede estar mediado por aminoácidos de cadena ramificada, insulina y factor de crecimiento similar a la insulina tipo 1 a través del complejo mTOR (diana de rapamicina en células de mamífero). Los estudios observacionales y los ensayos clínicos han demostrado que la disminución del contenido de proteína en los preparados para lactantes y de seguimiento puede reducir el riesgo de obesidad más adelante en la vida. El reciente conjunto de pruebas al respecto de esta teoría en la génesis de la obesidad y la DM2 se está traduciendo actualmente en nuevas políticas.
Además de la obesidad y sus complicaciones coexisten con carencias nutricionales específicas que también impactan de manera importante. Se observa que la deficiencia de diferentes micronutrimentos afectan el crecimiento y desarrollo fetal, deficiencias de hierro, zinc y calcio ocasionan adaptaciones hormonales y deficiencias de folato y vitamina B12 promueven una regulación epigenética significativa en esta etapa (Cuadros 8 y 9).
| Cuadro 8. Impacto sistémico por carencia de micronutrimentos | ||||
| Función renal | Función cardiovascular | Función célula beta | Función pulmonar | Composición corporal |
| Fe/Zn/Vit A/folato | Fe/Zn/Vit A/folato | Fe/Zn/Vit B12/folato | Vitaminas A y D | Fe/Zn/Vit B12/Mg/Ca/folato |
| Nefrogénesis alterada Filtración glomerular Sensibilidad al sodio |
Vascularidad alterada Malformaciones |
Reducción del número y área de células β | Modificación de ramificación broncoalveolar Menor elastina Capacidad pulmonar reducida |
Masa magra reducida Disposición grasa alterada Disregulación del apetito |
| Adaptado de: Gernand A, Schulze K, Stewart Ch, West K, Christian P. Micronutrient deficiences in pregnancy worldwide: health effects and prevention. Nat Rev. 2016;12(5):274-89. | ||||
| Cuadro 9. Resultados adversos para la salud de la deficiencia de micronutrientes gestacionales | |
| Corto Plazo | Largo Plazo |
| Aborto espontaneo | Muerte |
| Muerte prenatal | Alteraciones en el crecimiento, composición corporal |
| Defectos de nacimiento | Compromiso cardiometabólico, pulmonar y función inmune |
| Pequeño para le edad gestacional | Pobre neurodesarrollo y congnición |
| Nacimiento pretérmino | |
Nutrición temprana como riesgo y oportunidad. Acorde con lo anterior, la etapa preconcepcional está fuertemente vinculada al resultado del embarazo. La investigación señala a la salud antes de la concepción como crucial para la salud de generación en generación. Se observa que la malnutrición preconcepcional dada por déficit o excesos puede predisponer a riesgo de retraso en el desarrollo mental, trastorno de déficit de atención, hiperactividad, autismo, trastorno de desarrollo generalizado, discapacidad intelectual, tartamudez u otras, sin embargo, también es un periodo de oportunidad especial para la intervención en prevención. Además, la suplementación en el embarazo puede corregir deficiencias de nutrientes maternos, pero puede no ser suficiente para mejorar la salud infantil.
The Healthy Start Study evalúa la calidad de la dieta materna durante el embarazo y su impacto en la salud, observando que a menor índice de alimentación saludable en la madre, mayor cantidad de tejido adiposo neonatal. Asimismo, la ganancia excesiva de peso durante el embarazo, como ya se señaló, tiene un impacto que trasciende en la aparición de la enfermedad, sin embargo, importa mucho el momento del embarazo en donde se dé esa ganancia excesiva de peso; en otros estudios se observa que un exceso en la ganancia de peso durante el primero y segundo trimestres se asocia con mayor adiposidad, IMC y menos masa magra en la infancia.
Lactancia. Los efectos en la programación metabólica generados en la vida posnatal inmediata son cada vez más reconocidos por contribuir independientemente al desarrollo del síndrome metabólico en la edad adulta. La sobrealimentación durante el periodo de lactancia induce varias adaptaciones en los circuitos de energía en el hipotálamo de la descendencia, lo que los predispone a la aparición de la obesidad más adelante en la vida. Otro enfoque para una modificación nutricional en el periodo posnatal inmediato es el uso de fórmula láctea alta en hidratos de carbono (HC) sin cambios en la disponibilidad total de calorías, repercute en hiperinsulinemia casi inmediata después de su uso, la cual persiste en el periodo posterior al destete incluso después de la extracción de los HC de la fórmula. Las alteraciones significativas en los islotes pancreáticos apoyaron la hiperinsulinemia crónica de los lactados con la fórmula alta en HC. Las alteraciones en la expresión génica de neuropéptidos hipotalámicos que predisponen a la hiperfagia fueron evidentes durante el periodo con la dieta HC. Otros estudios han demostrado que la lactancia de una madre diabética, obesa o desnutrida resulta en una predisposición a la aparición de trastornos metabólicos en la descendencia.
Alimentación complementaria. Los determinantes del sobrepeso y la obesidad son complejos, pero la alimentación infantil y la dieta temprana son importantes factores contribuyentes. El periodo de alimentación complementaria en particular, es un tiempo durante el cual los niños son nutricionalmente vulnerables, y un tiempo en el que se pueden establecer hábitos alimentarios de por vida. La ingesta elevada de energía y proteínas, en particular la proteína láctea, en la infancia podría estar asociada con un aumento en el IMC y la grasa corporal. Existe cierta asociación entre el alto consumo de proteínas a los dos a 12 meses de edad y un índice de masa corporal más alto y aumento de masa grasa en la infancia, pero no fue el caso en todos los estudios. Una mayor ingesta de energía durante la alimentación complementaria se asocia con un mayor IMC en la infancia. Los estudios futuros deberían explorar el papel de la hormona de crecimiento e investigar si la ingesta de proteínas en la primera infancia afecta la salud más adelante en la vida.
Acciones a considerar en los primeros dos años de vida. La OMS recomienda la lactancia materna exclusiva hasta los seis meses de edad y la lactancia materna continua hasta los dos años de edad o más. Los alimentos complementarios apropiados deben introducirse de manera oportuna, comenzando cuando el bebé tenga seis meses de edad. En los países de bajos ingresos, la alimentación complementaria temprana o inadecuada puede conducir a la desnutrición y un crecimiento deficiente, pero en países como el Reino Unido y Estados Unidos, donde la obesidad es un problema de salud pública mayor que la desnutrición, la relación con el crecimiento no está clara. Estudios consideraron la relación entre el momento en que se introdujeron los alimentos complementarios y el IMC infantil, de los cuales algunos encontraron que la introducción de alimentos complementarios a menores de tres meses, cuatro meses o 20 semanas se asocia con un IMC más alto en la infancia. Otros estudios consideraron la asociación entre la alimentación complementaria y la composición corporal, se informó un aumento en el porcentaje de grasa corporal entre los niños que recibieron alimentos complementarios antes de las 15 semanas de edad. Huh et al., informaron que la introducción de alimentos sólidos antes de los cuatro meses se asoció con un aumento de casi seis veces en el riesgo de obesidad a los tres años entre los bebés alimentados con fórmula, pero no en los bebés amamantados al seno materno.
Independientemente de las experiencias tempranas de alimentación, los bebés destetados y listos para alimentos complementarios aprenden tanto a través de la exposición repetida (ocho a 10 exposiciones) a un alimento en particular como a la exposición a alimentos que varían en sabores y texturas; esto, a su vez, promueve la voluntad de comer no sólo los alimentos complementarios, sino también otros alimentos novedosos. Esta es una ventana de oportunidad para establecer una alimentación saludable.
En cuanto al consumo de jugo de frutas se observa que entre los niños que inicialmente tienen riesgo de sobrepeso o sobrepeso, el aumento en la ingesta de jugo de fruta se asocia con un aumento excesivo de la adiposidad, mientras que las frutas enteras se asocian con una ganancia reducida de la adiposidad.
Carga alostática y obesidad. La exposición a eventos o circunstancias estresantes tiene el potencial de contribuir a las respuestas psicosociales y fisiológicas que mantienen el equilibrio de todo el sistema, es un proceso llamado alostasis, función normal del cuerpo humano. La carga alostática (ALoad, por sus siglas en ingles), es una medida del estrés acumulativo en humanos que se ha asociado con un mayor riesgo de deterioro físico, mental y la tasa de mortalidad.
Se caracteriza por un deterioro gradual en la producción de insulina, por hiperglucemia y un estado de resistencia periférica a la insulina. Esta última condición explica la fuerte asociación clínica de la DM2 con la obesidad. La alteración de la secreción de insulina se ha demostrado en una variedad de estudios que revelan que adolescentes y adultos que padecen DM2 han perdido aproximadamente 80% de la función de sus células beta pancreáticas al diagnóstico de la enfermedad. En la mayoría de los casos, la disfunción pancreática no parece estar mediada por anticuerpos contra las células de los islotes pancreáticos como ocurre en DM tipo 1, aunque en esta variedad, la resistencia a la insulina puede estar presente en un grado variable, particularmente en asociación con la epidemia de sobrepeso y obesidad infantil.
Las dislipidemias son trastornos del metabolismo de las lipoproteínas que provocan una o más de las siguientes anormalidades (Cuadro 10).
| Cuadro 10. Concentraciones aceptables, limítrofes y anormales de lípidos plasmáticos, lipoproteínas y apolipoproteínas para niños y adolescentes | |||
| Categoría | Aceptable (mg/dL) |
Límite (mg/dL) |
Alto (mg/dL) |
| Colesterol total | < 170 | 170-199 | > 200 |
| C-LDL | < 110 | 110-129 | > 130 |
| C-No-HDL | < 120 | 120-144 | > 145 |
| Triglicéridos | |||
| De 0 a 9 años de edad | < 75 | 75-99 | > 100 |
| De 10 a 19 años de edad | < 90 | 90-129 | > 130 |
| C-HDL | > 45 | 40-45 | < 40 |
| Apo A-1 | > 120 | 115-120 | < 115 |
La etiología de las dislipidemias en pediatría incluye afecciones monogénicas, por ejemplo, hipercolesterolemia familiar (HF) y causas secundarias (Cuadro 11).
| Cuadro 11. Causas de dislipidemia secundaria en niños | |||
| Exógena | Endocrina/ metabÓlica | Renal | InfecciosA |
|
Obesidad central exógena
|
|
|
| HepÁticA | Enfermedad inflamatoria | Enfermedad de almacEnAMIENTO | Otros |
|
|
|
|
El síndrome metabólico (SM) es un término utilizado para describir la agrupación de factores de riesgo metabólico para DM2 y enfermedad cardiovascular aterosclerótica en adultos: obesidad abdominal, hiperglucemia, dislipidemia aterogénica (lípidos de alta densidad bajos e hipertrigliceridemia) e hipertensión arterial sistémicas. La coincidencia de riesgos cardiovasculares también ocurre en niños y adolescentes, particularmente en aquellos con obesidad. Las implicaciones que tiene el SM en el largo plazo deben ser consideradas en niños y adolescentes. Como resultado, la detección y el tratamiento deben centrarse en los factores individuales de riesgo cardiometabólico (obesidad, hiperglucemia, dislipidemia e hipertensión), al tiempo que se reconoce que a menudo se agrupan, por lo que deben abordarse en forma individual y en conjunto.
Los eventos de la ECV ateroscleróticos ocurren hasta la edad adulta, excepto en el contexto de trastornos genéticos raros, como la hipercolesterolemia familiar homocigótica. Sin embargo, el proceso aterogénico que conduce a la ECV comienza en la infancia y tal vez en la vida fetal, progresando a lo largo de la vida.
Aunque la aterosclerosis se desarrolla a una edad temprana, la ocurrencia real de un evento cardiovascular en la mayoría de los casos generalmente tardará decenios. El equipo de la Clínica de Obesidad y Enfermedades No Transmisibles (COyENT) del Instituto Nacional de Pediatría, realizó un estudio retrospectivo sobre los factores de riesgo presentados en la edad pediátrica y cuyos resultados aportaron información valiosa sobre el desarrollo de un nuevo paradigma en el entendimiento de la obesidad y sus alcances en morbimortalidad metabólica. Esto dio alcance al naciente concepto del síndrome heterocrónico sistémico por adiposidad visceral que los autores tratan de documentar en otras investigaciones. El uso de marcadores sustitutivos de ECV proporcionan una evaluación más conveniente, aunque menos directa del grado en que el riesgo en la infancia puede predecir el riesgo de ECV en la edad adulta. Numerosos estudios apoyan el uso del grosor íntima-media de la carótida (cIMT) como un predictor independiente de futuros eventos CV, incluso en adultos asintomáticos.
El Estudio de Salud Cardiovascular mostró una relación lineal entre cIMT y el riesgo relativo de eventos CV (definido como evento cerebrovascular o infarto de miocardio) en adultos sin ECV clínica y se sugirió como una herramienta para predecir independientemente eventos CV en adultos asintomáticos.
La presión arterial alta en niños y adolescentes es un problema de salud creciente que a menudo se pasa por alto. Los niños deben someterse a pruebas de detección de presión arterial elevada anualmente a partir de los tres años de edad o en cualquier edad si hay factores de riesgo. En niños menores de 13 años, la presión arterial elevada se define como la presión arterial en el percentil 90 o superior para la edad, la estatura y el sexo, y la hipertensión se define como la presión arterial en el percentil 95 o superior. En adolescentes de 13 años y mayores, la presión arterial elevada se define como una presión arterial de 120 a 129 mm Hg sistólica y menos de 80 mm Hg diastólica, y la hipertensión se define como una presión arterial de 130/80 mm Hg o más. Se debe realizar un control ambulatorio de la presión arterial para confirmar la hipertensión en niños y adolescentes.
La HTA en los niños se trata inicialmente con cambios en el estilo de vida, mejoría en el peso en caso de sobrepeso u obesidad, una dieta saludable y ejercicio regular. En niños con hipertensión sintomática (p. ej., cefalea, trastornos de la cognición y del aprendizaje); hipertensión en etapa 2 sin un factor modificable como la obesidad, evidencia de hipertrofia ventricular izquierda en la ecocardiografía, cualquier etapa de hipertensión asociada con enfermedad renal crónica o diabetes, o la hipertensión persistente a pesar de un ensayo de modificaciones en el estilo de vida, se requiere la prescripción de antihipertensivos y se debe evaluar el daño cardiovascular con ecocardiografía. Los inhibidores de la enzima convertidora de angiotensina (ECA), los bloqueadores de los receptores de angiotensina, los bloqueadores de los canales de calcio y los diuréticos tiacídicos son efectivos, seguros y bien tolerados en los niños.
La obesidad se asocia con un espectro clínico de anormalidades hepáticas conocidas colectivamente como enfermedad del hígado graso no alcohólico (NAFLD, por sus siglas en inglés) y que se ha constituido como la causa más común de enfermedad hepática en niños. Las anormalidades incluyen esteatosis (aumento de la grasa del hígado sin inflamación) y esteatohepatitis no alcohólica (NASH; aumento de la grasa del hígado con respuesta de inflamación). La historia natural de NASH en niños, en algunos casos, puede alcanzar estados de fibrosis, cirrosis y en última instancia, insuficiencia hepática.
La NAFLD representa un espectro de enfermedad del hígado graso que ocurre en ausencia de causas secundarias de esteatosis hepática, como el consumo de alcohol, hepatitis C, nutrición parenteral, medicación esteatogénica (p. ej., valproato), lipodistrofia o errores innatos del metabolismo.
Aunque la mayoría de los pacientes con NAFLD en la infancia se describen asintomáticos, la investigación intencionada de cada menor de edad con obesidad puede detectar dolor en el cuadrante superior derecho o síntomas inespecíficos, como molestias abdominales y fatiga. En el examen, la acantosis nigricans es común, lo que refleja la asociación entre NAFLD y resistencia a la insulina/diabetes tipo 2. Más frecuente de lo esperado los autores detectan hepatomegalia y/o hepatalgia, pero puede ser difícil determinarlo en el examen físico si hay una adiposidad abdominal significativa, y menos aún si no se establece una exploración orientada a este fin.
Las anormalidades de laboratorio en la NAFLD incluyen elevaciones en las transaminasas hepáticas (aminotransferasa de alanina [ALT] y aminotransferasa de aspartato [AST]), fosfatasa alcalina y glutamiltranspeptidasa gamma (GGTP). Estas anormalidades se resuelven o mejoran en niños con sobrepeso u obesidad que pueden reducir el exceso de adiposidad y mejorar su estado de peso a través de medidas de estilo de vida; aunque generalmente estas enzimas se encuentran elevadas en niños con NAFLD, pueden ser normales incluso en pacientes con evidencia histológica de esteatohepatitis no alcohólica (Cuadro 12).
| Cuadro 12. Definiciones y fenotipos de la enfermedad del hígado graso no alcohólico. Hipovitaminosis D | |
| Fenotipos | Definiciones |
| Enfermedad del hígado graso no alcohólico (NALFD) | Término incluyente que se refiere al espectro completo de la enfermedad |
| Indica infiltración grasa del hígado en ausencia de alcohol significativo, enfermedades genéticas o medicamentos que causan esteatosis | |
| La infiltración grasa generalmente se define como grasa > 5% del hígado mediante imágenes, cuantificación directa o estimación hepatológica | |
| Hígado graso no alcohólico | Esteatosis sin cambios específicos que sugieran esteatohepatitis, con o sin fibrosis |
| Esteatohepatitis no alcohólica pediátrica (NASH) | Esteatosis hepática con inflamación, con o sin lesión en globo a los hepatocitos y fibrosis |
| • Tipo 1 | Patrón de lesión centrada en la vénula (zona 3) o patrón confluente, generalmente con globo |
| • Tipo 2 | Patrón de lesión centrada en el portal predominante |
| NALFD con fibrosis | NAFLD o NASH con fibrosis peroportal, portal o sinusoidal o puente |
| NALFD con cirrosis | Cirrosis en el contexto de NAFLD |
El peso corporal excesivo y la obesidad en la infancia y la adolescencia se están convirtiendo en factores desfavorables cada vez más importantes que conllevan consecuencias extremadamente adversas y requieren la atención de nutriólogos clínicos y médicos de cualquier especialidad. Junto con la alta prevalencia de obesidad y síndrome metabólico en pacientes pediátricos, los niños y adolescentes en la mayoría de los países son diagnosticados con deficiencia de vitamina D. Entre los efectos no calciémicos de la vitamina D, su impacto en la regulación hormonal del metabolismo de la glucosa y la síntesis de adipocinas por el tejido adiposo desempeñan un papel importante. La revisión presenta datos de la literatura indicativos de una estrecha relación patogénica entre la insuficiencia de vitamina D y el deterioro en la sensibilidad a la insulina. Demuestra el papel de la insuficiencia de vitamina D en las reacciones inmunes que resultan en el desarrollo de inflamación subclínica en el tejido graso infiltrado con macrófagos y linfocitos. También muestra el papel de las adipocinas, las células del sistema inmunitario y las citocinas proinflamatorias producidas por ellas en la patogenia de la obesidad, así como la función de la vitamina D como regulador endocrino y paracrino del proceso de inflamación en el tejido adiposo. Las relaciones entre las principales adipocinas (leptina, adiponectina, resistina) se revelan en presencia de contenido normal de vitamina D y su deficiencia.
Gliosis hipotalámica inicial. El exceso energético debido al consumo de una alimentación alta en grasas desencadena una respuesta inflamatoria en el hipotálamo mediobasal (HMB), incluso antes de que inicie el aumento de peso afectando la función y el número de neuronas clave involucradas en el equilibrio energético, es decir, células propiomelanocórticas (POMC, por sus siglas en inglés). A corto plazo, la inflamación hipotalámica inducida por la alimentación conduce a la resistencia neuronal a factores anorexigénicos como la leptina y la insulina. Sin embargo, el consumo prolongado de alimentos altos en grasa puede conducir a un daño neuronal potencialmente irreversible, lo que aumenta la preocupación de que tales hallazgos subyacen a un control interrumpido de la homeostasis energética y las altas tasas de recurrencia de la obesidad. El efecto de inflamación en hipotálamo implica la activación y proliferación de células gliales, un proceso llamado gliosis.
Pseudotumor cerebri. La hipertensión intracraneal idiopática (IIH) también se conoce comúnmente como seudotumor cerebral (SC). Es un trastorno definido por criterios clínicos que incluyen síntomas y signos aislados de los producidos por el aumento de la presión intracraneal (p. ej., cefalea, papiledema, pérdida de visión), presión intracraneal elevada con composición normal de líquido cefalorraquídeo, y ninguna otra causa de hipertensión intracraneal evidente en estudios de neuroimagen u otras evaluaciones. El SC afecta principalmente a mujeres en edad fértil que tienen sobrepeso.
Una presentación típica del SC es la de una mujer adolescente o adulta joven con obesidad y que se queja de cefalea y a la exploración física intencional se le detecta edema de papila a través de un examen fundoscópico.
Síntomas: cefalea (84 a 92%); oscurecimientos visuales transitorios (68 a 72%); ruidos intracraneales (tinnitus pulsátil) de 52 a 60%; fotopsia 48 a 54%; dolor dorsal (53%), dolor retrobulbar (44%) y pérdida visual sostenida 26 a 32%.
Glomerulopatía. La obesidad produce anormalidades metabólicas complejas que tienen efectos de amplio alcance sobre las enfermedades que afectan los riñones. Algunas de las consecuencias deletéreas renales de la obesidad pueden estar mediadas por afecciones comórbidas posteriores, como diabetes mellitus o hipertensión, pero también hay efectos de la adiposidad que podrían afectar los riñones directamente, inducidos por la actividad endocrina del tejido adiposo a través de la producción de (entre otros) adiponectina, leptina y resistina. Éstos incluyen el desarrollo de inflamación, estrés oxidativo, metabolismo lipídico anormal, activación del sistema renina-angiotensina-aldosterona y aumento de la producción de insulina y su resistencia. La incidencia de la llamada glomerulopatía relacionada con la obesidad (ORG, por sus siglas en inglés) se ha multiplicado por 10 entre 1986 y 2000.
Nefrolitiasis. La resistencia a la insulina característica de la obesidad también puede predisponer a la nefrolitiasis a través de su impacto en el intercambio tubular de Na-H y la amoniagénesis, así como la promoción de un medio ácido y litiasis.
Cáncer renal. Los mecanismos detrás del aumento del riesgo de cáncer de riñón observado en personas obesas están menos caracterizados. La resistencia a la insulina, la consiguiente hiperinsulinemia crónica y numerosos efectos humorales secundarios complejos pueden ejercer efectos estimulantes sobre el crecimiento de varios tipos de células tumorales.
Ginecológicas. La obesidad infantil se asocia con el inicio temprano de la pubertad, las irregularidades menstruales durante la adolescencia y el síndrome de ovario poliquístico. Las mujeres en edad reproductiva con IMC altos tienen un mayor riesgo de problemas ovulatorios y tienden a responder mal al tratamiento de fertilidad. La pérdida de peso sostenido y sustancial es difícil de lograr con el estilo de vida y las medidas dietéticas disponibles actualmente (Cuadro 13).
| Cuadro 13. Impacto de la obesidad sobre la ginecología | |
| Condición | Impacto sobre adolescentes con obesidad |
| Pubertad | Inicio temprano |
| Síndrome de ovario poliquístico | Expresión fenotípica: incrementada |
| Infertilidad anovulatoria | Incrementada |
| Inducción de la ovulación | Requerimientos de la gonadotropina: incrementada |
| Pérdida de embarazo temprano | Incrementada |
| Seguridad anticonceptiva | Disminuida |
| Eficacia anticonceptiva | Disminuida |
| Irregularidades menstruales | Incrementadas |
| Incontinencia urinaria | Incrementada |
Urológicas y genitales. Se ha establecido una relación bidireccional entre el hipogonadismo y la obesidad, en gran parte debido a la compleja interacción entre las hormonas hipotalámicas y las adipocitocinas que controlan el eje hipofisiario-testicular. Por lo tanto, los cambios endocrinos asociados con la obesidad masculina pueden dar lugar a afecciones como la hipoandrogenia hipoestrogénica hipogonadotrópica, que puede afectar negativamente a la fertilidad al reducir la función testicular, modificar la espermatogénesis o reducir el deseo sexual.
La interrupción del eje HPG puede dar como resultado niveles reducidos de testosterona y aumentados de estrógeno. En el tejido adiposo, la testosterona se metaboliza a estradiol por la enzima aromatasa del citocromo P450, que realiza un paso clave en la biosíntesis de estrógenos y se expresa en niveles más altos, y con mayor actividad, en el tejido adiposo blanco. El aumento de la biodisponibilidad de la aromatasa en personas con obesidad da como resultado una mayor conversión de andrógenos en estrógenos, produciendo así simultáneamente mayores niveles de estrógenos circulantes.
Resultado de que el estrógeno es biológicamente más activo que la testosterona y los niveles anormalmente altos de estrógeno pueden provocar una retroalimentación negativa sobre el eje HPG a través de las neuronas de kisspeptina, los altos niveles de estrógeno en los hombres obesos resultan en una reducción en la producción de testosterona, lo que posteriormente afecta la espermatogénesis. Se ha planteado la hipótesis de que la secreción de kisspeptina podría ser la vía central que vincula la obesidad, la deficiencia de testosterona y los factores ambientales. Los estrógenos actúan además directamente sobre las pruebas para regular su función; diferentes modelos animales expuestos a altos niveles de químicos estrogénicos mostraron una reducción en el tamaño de las gónadas y una disminución en el conteo y la calidad de los espermatozoides en los varones.
Las únicas células somáticas directamente en contacto con las células germinales masculinas en desarrollo son las células de Sertoli, que proporcionan nutrientes y soporte. La adhesión de las células de Sertoli a las células germinales en desarrollo depende de la testosterona, con una reducción en la testosterona que conduce a la retención y la fagocitosis de las espermátides maduras. Además, la función epitelial en los túbulos seminíferos se ve afectada por la reducción de los niveles intratesticulares de testosterona, lo que afecta la espermatogénesis.
También se ha demostrado que los niveles bajos de testosterona se correlacionan con la obesidad general, el aumento de la circunferencia de la cintura y la mayor acumulación de grasa visceral.
Policitemia (eritrocitosis). Síndrome de Gaisböck. La policitemia se refiere a un aumento de la concentración de hemoglobina y/o hematocrito en la sangre periférica. El diagnóstico de la causa específica de policitemia es importante para el manejo adecuado del paciente. Los eritrocitos, como todas las células sanguíneas maduras, se derivan de células madre y progenitoras hematopoyéticas multipotenciales en la médula ósea a través de un proceso jerárquico de afectación y diferenciación de linaje.
Síndrome DIOS (Dysmetabolic Iron Overload Syndrome). El síndrome de sobrecarga de hierro dismetabólico (DIOS) corresponde a un aumento leve en las reservas de hierro en el hígado y en el cuerpo, asociadas con varios componentes del síndrome metabólico en ausencia de cualquier causa identificable de exceso de hierro. Se caracteriza por hiperferritinemia con saturación de transferrina normal o moderadamente aumentada, una o varias anormalidades metabólicas (aumento de la grasa visceral [Índice cintura-estatura > 0.50), presión arterial elevada, dislipidemia, metabolismo anormal de la glucosa, esteatohepatitis) y exceso leve de hierro hepático en resonancia magnética, imagenología o biopsia hepática. En 2019, el equipo de la COyENT del Instituto Nacional de Pediatría en México, documentó este hallazgo al estudiar la policitemia como marcador temprano de riesgo para el síndrome de apnea obstructiva del sueño (SAOS) en 698 niños atendidos en dicho servicio (Figuras 7 a 9).
Figura 7
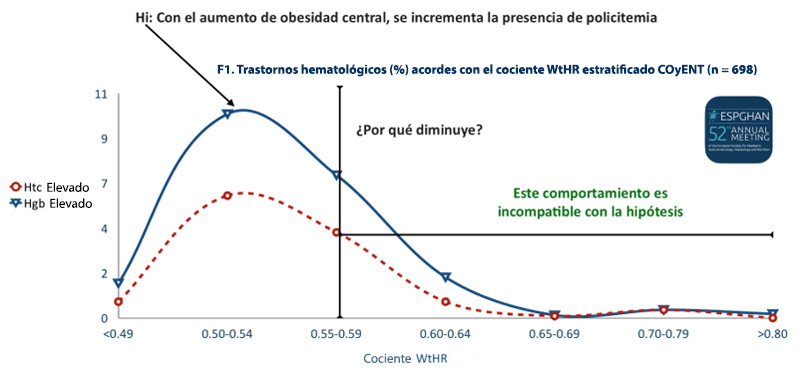
Síndrome DIOS en niños con sobrepeso y obesidad atendidos en la COyENT. [Perea Martínez A, Ríos Gallardo PT, Santiago Lagunes LM, Perea Caballero AL, Lara Campos AG. European Society for Paediatric of Gastroenterology, Hepatology and Nutrition. Glasgow. Scotland. 2019.]
Figura 8
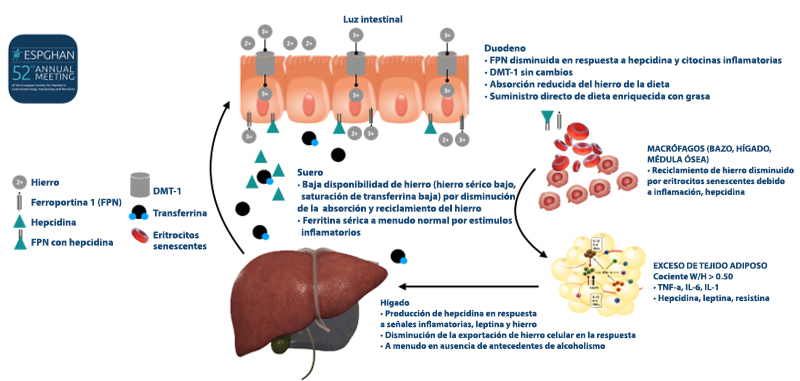
Mecanismo fisiológico del síndrome DIOS. [Perea Martínez A, Ríos Gallardo PT, Santiago Lagunes LM, Perea Caballero AL, Lara Campos AG. European Society for Paediatric of Gastroenterology, Hepatology and Nutrition. Glasgow. Scotland. 2019.]
Figura 9
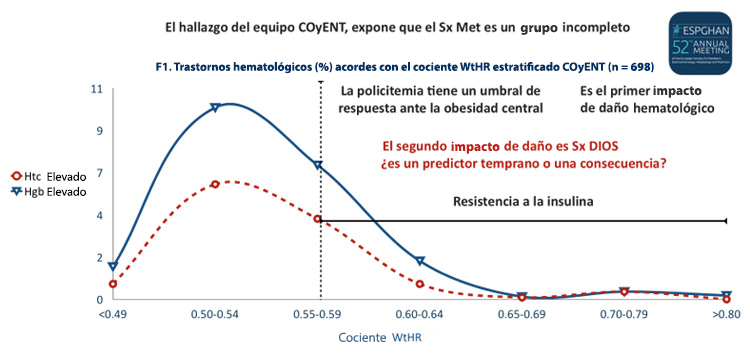
Hallazgo del síndrome DIOS en niños con sobrepeso y obesidad atendidos en la COyENT. [Perea Martínez A, Ríos Gallardo PT, Santiago Lagunes LM, Perea Caballero AL, Lara Campos AG. European Society for Paediatric of Gastroenterology, Hepatology and Nutrition. Glasgow. Scotland. 2019.]
Sepsis. Se caracteriza por alteraciones significativas en las citocinas y adipocinas circulantes, moléculas biológicamente activas producidas por el tejido adiposo, que están implicadas en procesos metabólicos e inflamatorios. Aunque los datos no son concluyentes con respecto a las adipocinas clásicas como la leptina y la adiponectina, la evidencia reciente ha puesto de relieve la notable elevación de la resistina y la visfatina en las enfermedades críticas y la sepsis, así como su asociación con la gravedad y los resultados de la sepsis (Cuadro 14).
| Cuadro 14. Rol de las adipocinas en la respuesta inflamatoria de la sepsis | ||
| Adipocina | Rol fisiopatológico | Acción inmunológica |
| Leptina | Regulador proinflamatorio | - Activación de macrófagos - Promoción de fagocitosis - Inducción de monocitos en IL-6 y TNF-α - Activación de quimiotaxis de neutrófilos - Diferenciación y sobrevivencia de célula T |
| Adiponectina | Antiinflamatorio | - Inhibición del crecimiento y macrófagos precursores - Supresión de la maduración de macrófagos - Inducción de IL-10 - Antagonismo de LPS - Inhibición de TLR4 - Supresión de las moléculas de adhesión |
| Resistina | Proinflamatorio | - Estimulación de células B y T - Inducción de IL-6, IL-8, IL-1β y TNF-α - Inhibición de macrófagos y apoptosis de neutrófilos - Activación de TLR4 - Regulación de la síntesis de NAD y explosión oxidativa (NAMPT intracelular) |
| Omentina-1 | Antiinflamatorio | - Inhibición de TNF-α - Inhibición de NF-κB, ICAM-1 y VCAM-1 |
| Chemerina | Regulador | - Factor quemotáctico - Posible acción antimicrobiana |
| Irisina (miocina y adipocina) | ¿Antiinflamatorio? | - Mejoramiento de la proliferación de macrófagos - Promoción de la fagocitosis - Inhibición temprana y tardía de mediadores inflamatorios (HMGB-1) |
| Fetuina-A (hepatocina y adipocina) | Antiinflamatorio | - Inhibición de la expresión de TNF-α - Inhibición de HMGB-1 - Inhibición de la expresión de citocinas en macrófagos - Inhibición de la expresión de citocinas en macrófagos - Opsonina para espermina - Mejoramiento de la fagocitosis |
La investigación realizada durante el último decenio ha demostrado que las vías inmunológicas y metabólicas están estrechamente relacionadas. Este emergente campo de inmunometabolismo incluye vías intrínsecas y extrínsecas y se reconoce su asociación con enfermedad metabólica acelerada por la obesidad. El inmunometabolismo intrínseco incluye el estudio tanto de la utilización de combustible y las vías bioenergéticas como de los productos que influyen en la función de las células inmunes. El inmunometabolismo extrínseco incluye el estudio de las células inmunes y de productos que influyen en el metabolismo sistémico. La inmunidad Th2, el manejo del hierro de los macrófagos, la memoria inmune adaptativa y la regulación epigenética de la inmunidad, que requieren cambios metabólicos intrínsecos, juegan un papel en el metabolismo sistémico y la función metabólica, uniendo los dos brazos del inmunometabolismo. Juntos, esto sugiere que atacar el inmunometabolismo intrínseco puede afectar directamente la función inmune y, en última instancia, el metabolismo sistémico.
Osteoporosis. La obesidad y la osteoporosis son problemas comunes de salud pública. Paradójicamente, mientras que la obesidad se asocia con una mayor densidad ósea, los individuos con diabetes tipo 2 con obesidad tienen un mayor riesgo de fractura. La asociación entre la obesidad y la densidad mineral ósea (DMO) se ve atenuada por la resistencia a la insulina, que se asocia con una DMO más baja. De hecho, la acumulación de evidencia clínica y experimental sugiere que la resistencia a la insulina, mediada por su asociación con la grasa visceral (ICE > 0.50), puede contribuir a la fisiopatología de la osteoporosis. El puntaje óseo trabecular (TBS, por sus siglas en inglés) es un parámetro de textura ósea que evalúa las variaciones de nivel de gris de píxeles en imágenes de absorciometría de rayos X de energía dual de la columna lumbar. El TBS es una medida indirecta independiente de la calidad ósea. TBS bajo refleja peor calidad ósea y micro-arquitectura afectada.
Existe una asociación bidireccional entre la sarcopenia y la obesidad en la patogenia de la sarcopenia (SO). Por un lado, una masa muscular esquelética baja puede conducir a tasas metabólicas en reposo reducidas y al gasto total de energía, promoviendo el aumento de grasa. Por otro lado, la obesidad puede favorecer el desarrollo y la progresión de la sarcopenia a través de una red multifactorial de alteraciones agrupadas. Se ha propuesto que la SO debiese ser más bien renombrada como sarcopenia por obesidad, para reflejar la dirección dominante de la ruta patogénica y capturar la noción de que la cascada patogénica de la SO se origina principalmente de disfunción e inflamación del tejido adiposo.
El sobrepeso y la obesidad se asocian con una amplia variedad de estigmatización y discriminación en la vida diaria. Las personas obesas tienen más dificultades para encontrar trabajo, tienen ingresos más bajos y se las ve con menos frecuencia en puestos de liderazgo. En la sociedad, la responsabilidad por la situación del peso es vista como una mentira por parte de los individuos afectados, lo que lleva a un estrés crónico, problemas de autoestima y percepción de pérdida de control. Como consecuencia, existe un mayor riesgo de desarrollar problemas psicológicos graves, como los trastornos afectivos y de ansiedad. Como reacción, se utilizan estrategias de afrontamiento para lidiar con la presión psicológica, como el comportamiento alimentario disfuncional, los atracones y la inactividad física. Mujeres, personas que pertenecen a otra minoría étnica o social, los adolescentes y las personas con trastornos alimentarios se consideran en mayor riesgo de angustia psicológica. Deben considerarse las vulnerabilidades psicológicas y las consecuencias de la estigmatización. Además, el control conductual percibido y la autoestima son aspectos clave que deben abordarse en el tratamiento.
SAHOS. La asociación entre el síndrome de apnea o hipoventilación del sueño (SAHOS) y la disfunción cardiovascular en la población pediátrica ha sido objeto de amplia investigación. Buena evidencia sugiere que la presencia de SAHOS en niños conduce a consecuencias adversas específicas para el sistema cardiovascular.
Tanto la disfunción cardiaca como la vascular están presentes en niños con SAHOS, y estas anormalidades parecen estar mediadas, directa o indirectamente, a través de cambios en vías específicas, incluidos los sistemas quimiorreflejo y barorreflejo, además de una respuesta inflamatoria sistémica. Como no se observan cambios en la estructura y función cardiovascular en todos los niños con SAHOS, es probable que otras señales genéticas y ambientales contribuyan a la progresión y gravedad de la enfermedad.
El SAHOS se caracteriza por episodios apneicos con diversos grados de hipoxemia e hipercapnia durante el sueño de movimiento ocular no rápido (NREM) y movimiento ocular rápido (REM). Estos episodios intermitentes de cesación parcial o completa del flujo de aire perturban el control autónomo normal del sistema cardiovascular. Además, las tasas de saturación de oxígeno y las elevaciones en los niveles de dióxido de carbono causan aumentos repentinos en la actividad simpática y los cambios cardiovasculares asociados. Los cambios de presión intratorácica durante el SAHOS también contribuyen a los efectos sobre el sistema cardiovascular. Las obstrucciones de las vías aéreas superiores que se producen con SAHOS, con contracciones diafragmáticas continuas, conducen a presiones intratorácicas excesivamente negativas que alteran la hemodinámica, como la poscarga del ventrículo izquierdo (VI).
La expansión de la aorta también se produce en presencia de estos cambios de presión intratorácica, movimiento que activa los barorreceptores y evita una mayor entrada simpática durante estos eventos de apnea. Los periodos alternos de respiración normal seguidos de apneas conducen a cambios episódicos en el llenado diastólico del VI, el volumen sistólico y el aumento de la resistencia vascular. Estos cambios culminan en una mayor variabilidad de la presión arterial (PA), a menudo en conjunción con cada evento de apnea. Se cree que la exposición crónica a fluctuaciones agudas anormales en la presión sanguínea durante e inmediatamente después del curso de cada evento de apnea conduce, eventualmente, a la pérdida de la "inmersión" nocturna normal en la PA nocturna promedio en comparación con la PA diurna. Durante meses o años, esto podría conducir a un mayor riesgo de hipertensión.
Los ácidos grasos poliinsaturados omega 3 poseen diversas cualidades a través de las cuales inciden directamente en los siguientes procesos:
Inflamación. Reducen la acción del factor nuclear kappa B (NF-κB), principal inductor genético para la síntesis de citocinas inflamatorias, con lo cual al inhibirse este factor, se reduce la respuesta inflamatoria.
Trombogénesis. Reducen la síntesis de tromboxano A2 (TXA2), la activación de adhesión de plaquetas, disminuyendo la actividad y concentración del inhibidor del activador del plasminógeno-1 (PAI-1).
Mejora de la dislipidemia. Triglicéridos y elevan las alfa-lipoproteinas (c-HDL).
Hipertensión. Inhibición de la enzima convertidora de angiotensina y aumenta la síntesis de óxido nítrico.
El ácido linoleico conjugado (CLA) es un término que describe un grupo de ácidos grasos con 18 átomos de carbono y los isómeros geométricos consisten en ácido linoleico. Este es un nombre común dado a un grupo de isómeros de posición con dos dobles enlaces separados por un grupo metileno. Esta conjugación del doble enlace está generalmente en las posiciones 9 y 11 ó 10 y 12, pueden ser una configuración cis o trans.
Sus funciones son inhibir al PPAR gamma necesario para diferenciar preadipocitos en adipocitos. Induce mayor actividad de la proteína desacoplante tipo 1 (UCP1) y con ello mayor termogénesis. Presumiblemente bloquea a propiomelanocortina y a neuropéptido, además del péptido relacionado con Agouti y con ello limita el hambre. Bloquea a lipoproteinlipasa y con ello la entrada de grasa al adipocito (Figura 10).
Figura 10
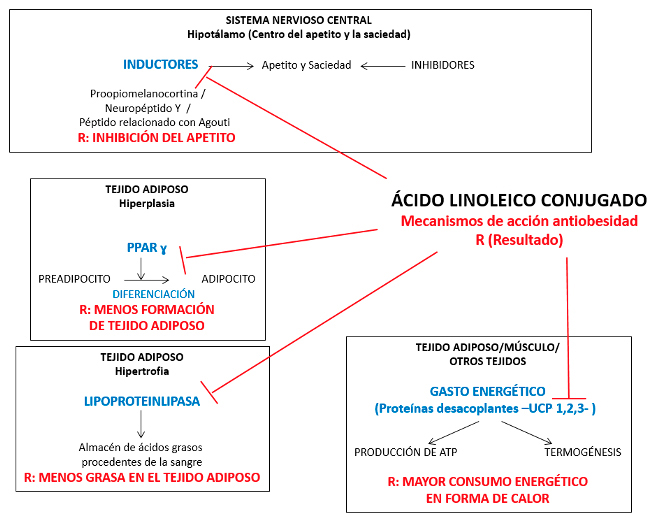
Mecanismos de acción del CLA.
El papel clásico de la vitamina D en la homeostasis del calcio y la salud esquelética ha sido ampliamente estudiado. En los últimos años, los niveles bajos de vitamina D se han asociado con afecciones no esqueléticas, como cáncer, enfermedades autoinmunes, resistencia a la insulina, síndrome metabólico, depresión y esquizofrenia. Las consecuencias de la deficiencia de vitamina D apuntan hacia la importancia de optimizar el estado de la vitamina D en la población general. La concentración sérica de (25 [OH] D) se considera el mejor biomarcador para la suficiencia de vitamina D. Según las pautas de 2010 del Instituto de Medicina (IOM por sus siglas en ingles), un nivel sérico de (25 [OH] D) > 50 nmol/L (20 ng/mL) se define como adecuado para 97.5% de la población. Este punto de ajuste se derivó de un compuesto de medidas de salud ósea. La cantidad diaria recomendada (RDA) de vitamina D3, definida por la IOM como la ingestión que cumple con el requisito de 97.5% de la población, se deriva de la respuesta a la dosis basada en los niveles séricos de (25 [OH] D).
La vitamina E tiene su papel fundamental a través de sus mecanismos de antioxidación, utilizada en dosis de 400 UI para la prevención de enfermedad cardiovascular y de 800 UI en el tratamiento de la enfermedad hepática grasa no alcohólica.
El estrés oxidativo induce modificaciones y alteraciones importantes en las funciones celulares. La obesidad a través de la producción excesiva de radicales libres facilita el estado de estrés oxidativo que redunda en el desarrollo de diversas complicaciones, en particular renales, cardiovasculares y metabólicas. El uso de vitamina C como un antioxidante demostrado es considerado en la prevención de ECV.
Edulcorantes no calóricos
Los edulcorantes no calóricos (ENC) son aditivos alimentarios cuya única función tecnológica es proporcionar sabor dulce a los alimentos, pero con un valor energético nulo o muy bajo, esta definición va de la mano con la que establece la Ley general de salud en cuanto a los aditivos, enfatizando que son sustancias permitidas, que no tienen propiedades nutritivas, que se pueden usar en la formulación de productos y que actúan modificando la estabilidad o conservación o características organolépticas del mismo para favorecer la apariencia o aceptabilidad.
Organismos nacionales e internacionales responsables de regular y garantizar la seguridad de los alimentos y bebidas para consumo humano, se han posicionado en la autorización de los ENC que cumplen perfectamente con los requisitos que ellos demandan. Entre éstos identificamos a la EFSA (Autoridad Europea de Seguridad Alimentaria), el Codex Alimentarius en donde intervienen la OMS y la FAO (Organización de las Naciones Unidas para la Alimentación y la Agricultura), el JECFA (Comité Mixto FAO/OMS de Expertos en Aditivos Alimentarios), la FDA y el Programa Internacional de Seguridad Química (IPCS). La seguridad de los ENC está avalada por cientos de estudios que establecen su estructura química, su metabolismo y absorción, sus efectos en el organismo, y sobre todo su seguridad toxicológica.
Los estudios que garantizan la seguridad en el consumo de ENC se basan además en las Guías de Buenas Prácticas de Laboratorio, resaltando el uso de un modelo animal apropiado, el cual se expone a grandes cantidades de aditivo de manera tanto aguda como crónica, se involucran estudios en varias generaciones considerando los efectos en las capacidades reproductivas y en el desarrollo fetal. Asimismo se examinan efectos de tipo observacional, funcional, bioquímico y patológico. Además, se administra el aditivo a niveles muy altos hasta obtener datos toxicológicos que permiten estimar los márgenes de seguridad de la exposición para determinar la toxicidad sistémica y llevar a cabo pruebas más específicas como de neurotoxicidad, inmunotoxicidad, entre otras.
Cada ENC tiene características químicas diferentes, que van de acuerdo a su origen, cómo se desarrolla su absorción, distribución, metabolismo y excreción (ADME), de tal manera que según esto presentan cualidades diferentes, las cuales son consideradas para su uso de manera aislada o en combinación con otros productos; a partir de esto, no se deben generalizar todos como si fueran iguales, sin atender a sus cualidades particulares, tanto para su uso como para sus observaciones durante la investigación o análisis de artículos (Cuadro 15).
| Cuadro 15. Características de los ENC | ||||
| Endulcorante no calórico | Capacidad endulzante* | ADME | Cualidades | IDA |
| Sucralosa 1976 | 600 veces más | Derivado policlorinado de la sacarosa (azúcar de caña) Se excreta sin cambios por heces y orina |
Estable en ambientes ácidos y en alta temperatura No cariogénico |
15 mg/kg. Seguro hasta con 16 000 mg/kg/día |
| Glicósidos de Esteviol (Rebaudiósidos A-D) 1899 | 200-300 veces más | Origen natural (Stevia rebaudiana) No se absorbe y se hidroliza por la microbiota intestinal a esteviol que se absorbe, se conjuga y se elimina por vía urinaria |
Estable, no fermentable y no cariogénica El Reb A es el más utilizado (pureza 95%) |
4 mg/kg/día con base en esteviol Reb A (12 mg/kg) Seguro hasta con 2 000 mg/kg/día |
| Aspartame* 1965 | 180 veces más | Se metaboliza en ácido aspártico, fenilalanina y metanol Se absorbe en intestino delgado y se excreta por vía renal sin ser metabolizado |
No en individuos con fenilcetonuria Termosensible No cariogénico |
30-40 mg/kg/día Seguro hasta con 4 000 mg/kg/día |
| Acesulfame–K 1966 | 150-200 veces más | Derivado del ácido acetoacético Absorción intestinal, excreción renal |
Sabor amargo Potencia el dulzor de otros ENC Termoestable |
15 mg/kg/día |
| Sacarina* 1879 | 300–500 veces más | Extracto purificado de las uvas No es metabolizado, se excreta por orina Se acumula en placenta |
Termoestable No aporta calorías |
5 mg/kg/día |
| Ácido ciclámico y sus sales (ciclamato) 1937 | 30–50 veces más | Se hidroliza por la microbiota intestinal a ciclohexilamina (CHA), una fracción se absorbe; se excreta sin cambios | Termoestable Buena solubilidad |
11 mg/kg/día |
| Neotame 1990 | 8 000-13 000 veces más | Resultado de la reacción de aspartame con dimetilburaldehído 20-30% se absorbe y se hidroliza por estearasas |
Reduce cantidad de fenilalanina Termoestable |
2 mg/kg/día |
| Luo Han Guo Monk Fruit (Fruta del monje) Glicósidos de cucurbitane (Mogrósidos II-VI) 1975* |
100-400 veces más Depende del contenido de Mogrósido V (25-95%) en el extracto |
Origen natural. (Siraitia grosvenorii) Se absorbe y está biodisponible sistémicamente Se excreta en la orina, mientras que sus metabolitos se excretan en las heces Conversión por enzimas digestivas y microbiota intestinal |
El Mogrósido V es el más utilizado Termoestable Potenciador de sabor |
Mogrósido V 2.2-2.5 mg/kg/día Seguro hasta con 1 717-2 062 mg/kg/día Extracto de fruta 1.6-6.2 mg/kg/día* Seguro hasta con 3 120-3 750 mg/kg/día* * Depende de la concentración de Mogrósido V |
| Adaptado de: Aldrete-Velasco J, López-García R, Zúñiga-Guajardo S, Riobó-Serván P, Serra-Majem L, et al. Análisis de la evidencia disponible para el consumo de edulcorantes no calóricos. Documento de expertos. Med Int Mex. 2017 enero;33(1):61-83. Wakida-Kuzunoki GH, Aguiñaga-Villaseñor RG, Avilés-Cobián R, Baeza-Bacab MA, Cavagnari BM, Del Castillo-Ruíz V, et al. Edulcorantes no calóricos en la edad pediátrica: análisis de la evidencia científica. Rev Mex Pediatr 2017;84(supl 1):S3-S23. Scientific opinion EFSA. Safety of use of Monk Fruit extract as a food additive in different food categories. EFSA Journal 2019. GRAS Notice (GRN). Determination of the generally recognized as safe (GRAS) Status of Siraitia Grosvenori Swingle (Luo Han Guo) fruit extract as a food ingredient. GNR 2017. | ||||
En cuanto a la aplicación de los ENC como un recurso de transición a lo saludable, existen diferentes estudios en niños, adolescentes y adultos que lo fundamentan. Se ha observado que reemplazar bebidas con azúcar por bebidas con ENC ayuda a disminuir hasta 30% la ingesta calórica total, hay menor ganancia de peso y masa grasa, ayudan a disminuir el peso hasta 5% en seis meses comparándolo sólo con cambios en la alimentación, hay dos veces más probabilidad de perder peso igual que el reemplazarlas por agua y se ha demostrado tener mejor adherencia a la propuesta de intervención.
Su uso combinado con programas de intervención impacta en la disminución de peso corporal, menor masa grasa, de la circunferencia de cintura y reducción de 5% de peso total y cintura incluso comparándolo con el agua.
Otras observaciones alrededor de los ENC y su aplicación han sido aclaradas en más estudios, se ha demostrado que no aumentan el peso corporal ni la masa grasa, tienen un impacto neutro o de disminución del IMC a corto plazo, no tienen una dulzura máxima o intensidad de dulzor mayor que la sacarosa o azúcar de mesa, se ha demostrado que en su mayoría estimulan los receptores amargos y con ello ayudan a establecer un límite de ingesta; finalmente no influyen en la preferencia de alimentos o en la regulación de la ingesta a corto y mediano plazos.
En un estudio realizado en la Clínica de Obesidad y Enfermedades no Transmisibles del INP se evaluó un modelo de intervención basado en la promoción y reforzamiento de hábitos saludables con citas frecuentes, primero ocho citas semanales y luego seis citas mensuales con un equipo multidisciplinar capacitado. El modelo de intervención intensiva utilizado en la atención de los menores de edad incluidos en el estudio, demostró un efecto benéfico sobre las conductas de riesgo, al lograr reducir el sedentarismo, optimizar el hábito del desayuno, contener el exceso en las porciones alimentarias o su repetición, mejorar los patrones de la alimentación y sus constituyentes, elevar el consumo de frutas y verduras; también logró incrementar el consumo de agua, reducir el consumo de bebidas y de alimentos hiperenergéticos. En los resultados de este estudio se observa una mejoría importante a un primer corte a las ocho semanas de intervención y un corte final al 8º mes de atención, demostrando una reducción del peso corporal, de la circunferencia de cintura, el índice de masa corporal y del índice cintura-estatura, considerados el 2º y 4º como los mejores indicadores de adiposidad visceral y, por ende, de riesgo sistémico. El resultado se hace más evidente gracias a que es favorecido por el crecimiento lineal que presentan los niños. Haciendo un análisis individual de cada corte. El resultado obtenido a las ocho semanas revela una mejora en todos los hábitos alimentarios, en particular el hábito de consumir bebidas hiperenergéticas endulzadas que estaba presente en el 100% de los individuos de estudio, se redujo a sólo el 18% de ellos a esta etapa de evaluación. Es de llamar fuertemente la atención, que al segundo corte la recaída en el hábito de consumo de bebidas endulzadas fue altamente significativo, recuperándose hasta un 62.5%, lo que señala la dificultad de abandonar este hábito y haciendo necesario considerar el uso de edulcorantes no calóricos para evitar el impacto de la recaída en los índices e indicadores de adiposidad (Figura 11).
Figura 11
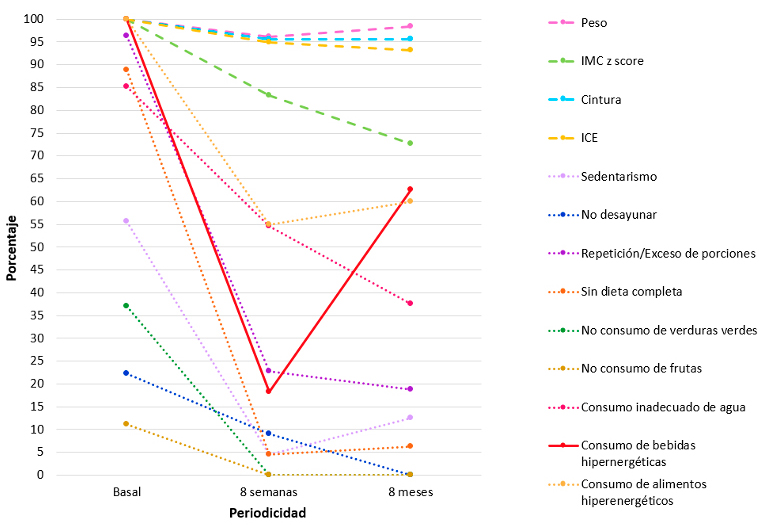
Resultados de la intervención 8x8 de la COyENT.
La obesidad y las enfermedades no transmisibles (ENT) constituyen un grupo de entidades clínicas que se originan y desarrollan desde la vida prenatal, incluso la preconcepcional.
Los alcances epigenéticos del estado nutricional de los nuevos progenitores y en particular de la gestante, traduce la influencia de diversos macronutrimentos y micronutrimentos en la estructura y la función celular, orgánica y sistémica en el corto y largo plazos.
La obesidad como una entidad inflamatoria de bajo grado, establece una línea de procesos degenerativos en las que además de la inflamación, el estrés oxidativo y los procesos apoptoicos determinan un riesgo temprano de morbilidad y mortalidad. En la infancia y en la adolescencia, los individuos con obesidad requieren de una evaluación extensa enfocada a detectar complicaciones y tratarlas.
La nutrición del individuo sano y enfermo es un factor que determina en todo momento de la vida, procesos de equilibrio o desajuste según la condición, que impactan en preservar, recuperar o mejorar la salud.
Los nutrimentos como instrumento terapéutico adyuvante en la obesidad y en las ENT está posicionándose en forma gradual como un recurso fundamental en el tratamiento integral de estos padecimientos.
Los ácidos grasos poliinsaturados omega 3 representan una estrategia nutriterapéutica para contener el riesgo cardiovascular y neurodegenerativo de las enfermedades no transmisibles.
El ácido linoleico conjugado, un AGPI n 6 se ha colocado en el grupo de nutrimentos con efectos antiobesidad demostrados pero debe asentarse que tiene una calidad de adyuvante y de ninguna forma sustituye a un mejor estilo de vida.
La vitamina D como un nutrimento pleiotrópico de alto impacto epigenético y regulador funcional sistémico, se establece como un recurso de evaluación necesaria en los casos de obesidad y de ENT.
En un contexto más clínico que traslacional, el profesional de la salud habrá de evaluar las aportaciones de las ciencias básicas en el terreno de la nutrición con un enfoque a mejorar y enriquecer sus estrategias de prevención y tratamiento de la obesidad y de las ENT.
Los ENC cuentan con un soporte científico para ser usados en personas con obesidad y sus complicaciones metabólicas, como un recurso de transición de un balance energético de riesgo hacia uno saludable.